Хронический вирусный гепатит в у взрослых. Гепатит B, HBV-инфекция печени, лечение
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК - 2015
Хронический вирусный гепатит b без дельта-агента (B18.1), Хронический вирусный гепатит b с дельта-агентом (B18.0)
Гастроэнтерология
Общая информация
Краткое описание
Экспертным советом
РГП на ПХВ «Республиканский центр развития здравоохранения»
Министерства здравоохранения и социального развития Республики Казахстан
Протокол № 10
Хронический гепатит В
- некровоспалительное заболевание печени, вызванное вирусом гепатита В, характеризующееся наличием определяемого поверхностного антигена вируса гепатита В (HBsAg) в крови или сыворотке длительностью более 6 месяцев .
I. ВВОДНАЯ ЧАСТЬ
Название протокола:
Хронический вирусный гепатит В у взрослых.
Код протокола:
Код(ы) МКБ-10:
B 18.1 - Хронический гепатит В без дельта агента;
B 18.0 - Хронический гепатит В с дельта агентом.
Сокращения, используемые в протоколе:
АЛТ - аланинаминотрансфераза
AMA - антимитохондриальные антитела
АН - аналоги нуклеозидов/нуклеотидов
АСТ - аспартатаминотрансфераза
АФП - альфа-фетопротеин
ВГВ - вирусный гепатит B
ВГН - верхняя граница нормы
ВГС - вирусный гепатит С вирусный гепатит С
ВГD - вирусный гепатит D
ВИЧ - вирус иммунодефицита человека
ВРВ - варикозно-расширенные вены
ГТП - гамма-глутамилтранспептидаза
ГЦК - гепатоцеллюлярная карцинома
ДНК - дезоксирибонуклеиновая кислота
ИМТ - индекс массы тела
ИАГ - индекс гистологической активности
ИСТ - иммуносупресивная терапия
ИФА - иммуноферментный анализ
ИХА - иммунохимический анализ
КТ - компьютерная томография
МЕ - международные единицы
Мл - миллилитр
МНО - международное нормализованное отношение
МРТ - магнитно-резонансная томография
ОАК - общий анализ крови
ОАМ - общий анализ мочи
ОБП - органы брюшной полости
ПБП - пункционная биопсия печени
ПВ - протромбиновое время
ПВТ - противовирусная терапия
ПЕГ-ИНФ - пегилированный интерферон
ПЦР - полимеразная цепная реакция
РК - Республика Казахстан
РНК - рибонуклеиновая кислота
СОЭ - скорость оседания эритроцитов
ТП - трансплантация печени
ТТГ - тиреотропный гормон
УЗИ - ультразвуковое исследование
УЗДГ - ультразвуковая допплерография
ХГ - хронический гепатит
ХГВ - хронический гепатит В
ХГD - хронический гепатит D
ХГС - хронический гепатит C
ЦП - цирроз печени
ЩФ - щелочная фосфатаза
ЭГДС - эзофагогастродуоденоскопия
ЭКГ - электрокардиограмма
УД - уровень доказательности
ANA - антинуклеарные антитела
Anti-HBc /IgM - антитела к HBcAg класса М
Anti-Hbe - антитела к HBeAg
Anti-HBs - антитела к HBsAg
Anti-HCV - антитела к вирусу гепатита C
Anti-HDV - антитела к вирусу гепатита D
Anti-HDV IgM - антитела к вирусу гепатита D класса М
Anti-HIV - антитела к ВИЧ
Anti-НВс /IgG - антитела к HBcAg класса G
APRI - индекс соотношения АСТ к числу тромбоцитов
ETV - энтакавир
HAV - вирус гепатита А
HBcAg - сердцевинный или ядерный антиген гепатита В
HBeAg - внутренний антиген вируса гепатита В
HBsAg - поверхностный антиген вируса гепатита В
HBV - вирус гепатита В
HBV ДНК - ДНК ВГВ
HCV - вирус гепатита С
HCV РНК - РНК ВГС
HDV - вирус гепатита D
HDV РНК - РНК ВГD
IgG - иммуноглобулины класса G
IQR - интерквартальный коэффициент
IU - международные единицы
NICE - National Institute for Health and Care Excellence
F - фиброз
FDA - Food and Drug Administration - Управление по санитарному надзору за качеством пищевых продуктов и медикаментов
LAM - ламивудин
LdT - телбивудин
LBx - биопсия печени
MELD - Model for End-stage Liver Disease
Log - логарифм
Дата разработки протокола
: 2015 год.
Пользователи протокола
: гастроэнтерологи, инфекционисты, хирурги, трансплантологи, онкологи, нефрологи, терапевты, врачи общей практики.
Оценка на степень доказательности приводимых рекомендаций.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика |
Классификация
Клиническая классификация
Общепринятая классификация отсутствует.
При постановке диагноза необходимо указать вирусологический статус (HBeAg-позитивный или HBeAg-негативный статус, вирусную нагрузку, наличие дельта-агента), активность (биохимическую и/или гистологическую), а также стадию заболевания (по данным непрямой эластографии или морфологического исследования) .
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне
(исследования, необходимые для всех пациентов с ВГВ):
1. ОАК с подсчетом тромбоцитов;
2. Биохимический профиль: АЛТ, АСТ, щелочная фосфатаза, общий билирубин, прямой билирубин, непрямой билирубин, ГГТП, альбумин, креатинин.
3. Коагулограма: МНО или ПВ;
4. Серологические исследования (методом ИХА/ИФА): HBsAg (качественный тест), HBeAg, anti-HBs, anti-HBe, anti-HBc /IgM, anti-НВс /IgG, anti-HDV IgM, anti-HDV total, anti-HCV, anti-HIV.
6. Молекулярная диагностика на основе полимеразной цепной реакции:
7. Ультразвуковое исследование органов брюшной полости (УЗИ ОБП): печень, селезенка, желчный пузырь, поджелудочной железы;
8. Непрямая эластография.
Дополнительные диагностические обследования, проводимые на амбулаторном уровне:
Биохимический профиль:мочевина, калий, натрий, гамма-глобулины, общий холестерин, триглицериды, глюкоза, сывороточное железо, ферритин, аммиак;
Церулоплазмин;
Тест на беременность;
Осмотр глазного дна.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию : согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне:
ОАК с подсчетом тромбоцитов;
Биохимический профиль: АЛТ, АСТ, щелочная фосфотаза, общий билирубин, прямой билирубин, ГГТП, альбумин, креатинин.
Коагулограмма: МНО или ПВ;
Серологические исследования (методом ИХА/ИФА):HBsAg (качественный тест), HBeAg, anti-HBs, anti-HBe, anti-HBc /IgM, anti-НВс /IgG, anti-HDV IgM, anti-HDV total, anti-HCV, anti-HIV.
Молекулярная диагностика на основе полимеразной цепной реакции:
Определение HBV-ДНК (качественный тест);
При положительном результате качественного теста HBV-ДНК - количественное определение HBV-ДНК;
При наличии anti-HDV - определение HDV-РНК (качественный тест)
При положительном результате качественного теста HDV-РНК - количественное определение HDV-РНК;
Ультразвуковое исследование органов брюшной полости (УЗИ ОБП): печень, селезенка, желчный пузырь, поджелудочной железы;
Непрямая эластография.
Дополнительные диагностические обследования, проводимые на стационарном уровне:
Биохимический профиль: мочевина, калий, натрий, гамма-глобулины, общий холестерин, триглицериды, глюкоза, сывороточное железо, ферритин, аммиак;
HBsAg (количественный тест);
Церулоплазмин;
Функциональные пробы щитовидной железы: ТТГ, Т4 свободный, Ат к ТПО;
Тест на беременность;
УЗДГ сосудов печени и селезенки;
КТ органов брюшной полости (при подозрении на объёмные образования и тромбозы - с в/в контрастированием);
МРТ органов брюшной полости (при подозрении на объёмные образования и тромбозы - с в/в контрастированием;)
Осмотр глазного дна.
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: нет.
Диагностические критерии постановки диагноза
Жалобы и анамнез
Первоначальная оценка пациентов с хроническим гепатитом В должна включать тщательный сбор жалоб, анамнеза и физикальное обследование, с акцентом на факторы риска, таких как ко-инфекции, употребление алкоголя, семейная история инфекции ВГВ и рака печени (УД - А).
Жалобы
Хронический гепатит В часто протекает бессимптомно на ранних стадиях заболевания; могут быть недомогание; усталость.
На более поздних стадиях появляются симптомы, связанные с портальной гипертензией и терминальной стадии заболевания печени (желтуха, энцефалопатия, асцит, кровотечение из варикозных узлов и т.д.).
Хронический гепатит В может быть ассоциирован с внепеченочными проявлениями, такими как: апластическая анемия, папулезный акродерматит, синдром Шегрена, кожный васкулит, узелковый полиартериит, полиартралгии, миалгии, миокардит, гломерулонефрит, фиброзирующий альвеолит, криоглобулинемия и др.
Анамнез
Необходимо уточнить следующие факторы риска заражения HBV-инфекцией :
Иммиграция из эндемичных стран по HBV-инфекции;
Наличие у родителей HBV-инфекции;
Контакт с HBV-носителем;
Сексуальный контакт с HBV-носителем, HIV;
Большое количество сексуальных партнеров;
Мужчины, имеющие половые контакты с мужчинами;
Использование в прошлом или в данный момент внутривенных наркотиков;
Пребывание в местах заключениях;
Проведение диализа;
Переливания крови, оперативные вмешательства, трансплантация органов и тканей.
Физикальное обследование
При физикальном осмотре можно не обнаружить никаких специфических признаков или выявить стигмы хронического заболевания печени: желтуху гепатомегалию, спленомегалию (10%), пальмарную эритему, сосудистые звездочки, полиартрит. При развитии цирроза печени отмечаются симптомы, обусловленные дисфункцией печени и портальной гипертензией.
Лабораторные исследования :
. ОАК с подсчетом тромбоцитов (УД - А) проводится в целях диагностики гиперспленизма (цитопении), выявления анемии (различно этиологии), выявления показателей системного воспалительного ответа, а также определения противопоказаний и мониторинга побочных явлений ПВТ.
. Биохимический анализ крови
необходим для определения следующих биохимических синдромов (УД - А):
− Синдром цитолиза: повышение активности АЛТ, АСТ. По уровню АЛТ выставляется степень биохимической активности (Таблица№2).
Таблица 2
. Степень биохимической активности
− Синдром холестаза: повышение активности ЩФ, ГТП, уровней прямого билирубина, холестерина;
− Синдром печеночно-клеточной недостаточности: гипоальбуминемия, увеличение МНО, ПВ.
− Синдром шунтирования: повышение уровня аммиака.
− Синдром иммунного воспаления: ускорение СОЭ, гипергамма-глобулинемия, наличие аутоантител.
Кроме того, по биохимическому анализу крови проводят оценку тяжести заболевания печени:
− уровень АЛТ, как правило, выше, чем уровни АСТ, но соотношение может меняться при прогрессирующем фиброзе и циррозе;
− характерные признаки цирроза — прогрессирующее снижение уровня альбумина плазмы, удлинение протромбинового времени, снижением числа тромбоцитов.
. Альфа-фетопротеин (АФП) используется в качестве скринингового теста ГЦК . (УД - А).
. Показатели сывороточного железа и ферритина
необходимы в целях исключения гемохроматоза и синдрома вторичной перегрузки железом.
. Серологическая диагностика
проводится с использованием иммунохемилюминисцентного анализа (ИХА), при отсутствии ИХА - иммуноферментного анализа (ИФА); вирусологическая диагностика HBV-инфекции (в целях определения репликации вируса) проводится на основе полимеразной цепной реакции (качественный тест, при положительном результате - количественный) с использованием автоматизированных систем закрытого типа в режиме реального времени с нижним лимитом определения 6-10 МЕ/мл.
На основе серологической и вирусологической диагностики определяется фаза HBV-инфекции .
В естественном течении хронического вирусного гепатита В выделяют несколько фаз (Таблица№3, Рисунок №1):
− Иммунотолерантная
− Иммунореактивная (иммунного клиренса или HBeAg-позитивный ХГВ)
− Неактивное носительство HBsAg (низкорепликативная)
− HBeAg-негативный ХГВ (реактивации)
− HBsAg-негативная (паст-инфекция HBV, оккультный ХГВ)
Установление фазы ХГВ важно для определения прогноза заболевания и показаний к противовирусной терапии.
Таблица №3
. Фазы хронического вирусного гепатита В.
| Фазы | HBsAg | Anti-HBs | HBeAg | Anti-HBe | HBV DNA | АЛТ | Гистология | |
| 1. Иммунотолерантная (чаще и длиннее при перинатальном заражении) | + | -- | + | N | N | |||
| 2. Иммунореактивная (HBeAg-позитивный (недели-годы) | + | -- | + | |||||
| 3. Неактивное носительство HBsAg |
<1000 МЕ/мл |
-- | -- | + |
+/-- <2000 (иногда до 20000) МЕ/мл |
N | N | |
| 4. HBeAg-негативный ХГВ | + | -- | -- | + | Активный гепатит, прогрессирующий фиброз | |||
| 5. HBsAg-негативная | Паст-инфекция HBV | -- | +/-- | -- | + | -- | N | N |
| Оккультный ХГВ | -- | + | -- | + | В печени: +; в сыворотке: +/-- (<200 МЕ/мл) | N/ | Гепатит, фиброз | |
Рисунок№1 . Диагностика и естественное течение ХГВ
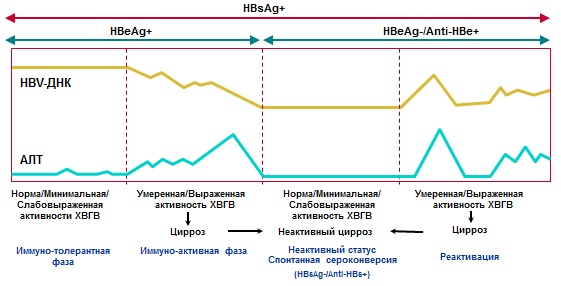
Необходимо также проводить поиск других возможных причин хронического заболевания печени, включая ко-инфекцию HDV (определение anti-HDV строго обязательно у всех пациентов с HBV-инфекцией), HCV и/или ВИЧ. У пациентов с хронической HBV-инфекцией требуется также определять антитела к вирусу гепатита А (анти-HAV), а при их отсутствии следует рекомендовать вакцинацию против HAV-инфекции.
Инструментальные исследования
УЗИ
позволяет оценить структуру печени, признаки фиброза, перехода цирроза печени (неровный край, нодулярная структура, атрофия правой доли, наличия асцита, расширение и тромбоз сосудов печени и селезенки, наличие шунтов, спленомегалия и другие признаки портальной гипертензии), а также наличие объемных образований (ГЦК и др.) (УД - А). Для уточнения изменений кровотока целесообразно использование УЗДГ.
Другие лучевые методы исследования (КТ или МРТ с внутривенным контрастным усилением) используются для верификации объемных образований и тромбозов .
Эндоскопические исследования необходимы для диагностики ВРВ пищевода и желудка, портальной гастропатии, других сопутствующих поражений слизистой оболочки гастродуоденальной зоны, а также выявления расширения геморроидальных вен.
Диагностика стадии фиброза проводится с помощью пункционной биопсии печени и неинвазивных методик
(НЭ, биомаркеров: исчисляемых индексов и зарегистрированных коммерческих наборов).
Пункционная биопсия печени (ПБП) для определения степени воспаления, некроза и фиброза рекомендуется пациентам, т. к. сведения о морфологических изменениях печени могут оказаться полезными при принятии решения о начале терапии (УД - А). Биопсия также может помочь выявить другие возможные причины поражения печени, такие как стеатоз, стеатогепатит, атоиммуный гепатит и т.д. Несмотря на то, что биопсия печени - инвазивная процедура, риск тяжелых осложнений крайне низок (1:4000-10 000) . Очень важно, чтобы при пункционной биопсии размер получаемого образца был достаточным для точного суждения о степени поражения печени и выраженности фиброза.
Пункционная биопсия печени для уточнения стадии фиброза может быть рекомендована пациентам с результатами НЭ в области серой зоны (от 6 до 10 кРа).
В ряде случаев, проведение биопсии целесообразно при результатах НЭ меньше 6 кПа у пациентов в возрасте младше 30 лет с уровнем ДНК HBV выше 2000 МЕ/мл и повышенным уровнем АЛТ (≥ 30 МЕ/л у мужчин и ≥ 19 МЕ/л у женщин) по результатам 2 анализов, проведённых с интервалом в 3 месяца.
Биопсия обычно не требуется у больных с клиническими признаками цирроза печени, а также у пациентов, которым терапия показана независимо от степени активности процесса и стадии фиброза. Проведение пункционной биопсии также не рекомендуется пациентам с результатами транзиторной эластографии менее 6кПа, нормальной активностью АЛТ и уровнем HBV-ДНК < 2000 МЕ/мл, так как вероятность серьёзного поражения печении и необходимости проведения противовирусной терапии у таких пациентов крайне мала.
Оценка результатов ПБП проводится с применением полуколичественных шкал описания степени некровоспалительных изменений и стадии фиброза ткани печени (см. Таблицы 4 и 5).
Таблица 4
. Морфологическая диагностика степени некровоспалительной активности гепатита
| Диагноз гистологический | METAVIR | Knodell (IV) | Ishak |
| ХГ минимальной активности | А1 | 0-3 | 0-3 |
| ХГ слабовыраженной активности | А1 | 4-5 | 4-6 |
| ХГ умеренной активности | А2 | 6-9 | 7-9 |
| ХГ выраженной активности | А3 | 10-12 | 10-15 |
| ХГ выраженной активности с мостовидными некрозами | А3 | 13-18 | 16-18 |
Таблица 5 . Морфологическая диагностика стадии заболевания печени (выраженности фиброза)
| Стадия фиброза |
METAVIR* |
Knodell (IV) | Ishak |
| Нет фиброза | F0 | 0 | 0 |
| Портальный фиброз нескольких портальных трактов | F1 | 1 | 1 |
| Портальный фиброз большинства портальных трактов | F1 | 1 | 2 |
| Несколько мостовидных фиброзных септ | F2 | 3 | 3 |
| Много мостовидных фиброзных септ | F3 | 3 | 4 |
| Неполный цирроз | F4 | 4 | 5 |
| Полностью сформировавшийся цирроз | F4 | 4 | 6 |
*Для определения стадии заболевания печени чаще применяется шкала METAVIR
Непрямая эластография (НЭ) имеет большее клиническое значение, чем сывороточные биомаркеры фиброза печени . Позволяет судить об изменении эластических свойств печени на основании отраженных вибрационных импульсов и последующего их компьютерного анализа. Интерпретация результатов непрямой эластографии представлена в Таблице №6. Значение от <5-6 кПа часто указывает на отсутствие или минимальной степени фиброз печени , а > 12-14 кПа часто указывает на цирроз печени. В сомнительных случаях, если это повлияет на тактику ведения больного, рекомендуется биопсия печени (схема №1). Среди больных хроническим гепатитом В с повышением уровня АЛТ, интерпретация данных НЭ должны проводиться с осторожностью, так как данные могут быть завышенными, даже в течении 3 - 6 месяцев после нормализации АЛТ .
Таблица 6 . Интерпретация результатов непрямой эластографии
Интерпретация результатов эластометрии затруднена в случаях (УД - А):
Избыточного веса (ИМТ>35 кг/м2)
Выраженного стеатоза печени
Высокой биохимической активности (АЛТ/АСТ выше верхнего лимита нормы в 3 и более раз)
Критерии успешного результата исследования:
Интерквартильный коэффициент (IQR) - не более 30% показателя эластичности.
Не менее 10 достоверных измерений в одной точке исследования
Не менее 60% успешных измерений.
Биомаркеры включают:
Индексы фиброза. Неинвазивные маркеры фиброза печени могут дать более развернутую оценку поражения печени . Эти методы более безопасные и дешевле, чем биопсия печени. Тест APRI (УД - А) использует только два параметра: АСТ и количество тромбоцитов .
Формула расчета
: APRI = * (AST/ULN) x 100) / platelet count (109/L)
0,3 - 0,5 исключают значимый фиброз и цирроз
>1,5 указывают на клинически значимый фиброз
Электронный калькулятор : www.hepatitisc.uw.edu/page/clinical-calculators/apri
Схема №1

Показания для консультации узких специалистов:
Консультация офтальмолога состояние глазного дна) - до и во время ПВТ;
Консультация психиатра - до, перед, во время при подозрении на депрессию;
Консультация дерматолога;
Консультация аллерголога - при наличии кожных/аллергических и аутоиммунных реакций;
Консультация онколога - при подозрении на ГЦК;
Консультация хирурга - трансплантолога - в случаях наличия показаний к ТП.
Дифференциальный диагноз
Дифференциальный диагноз с наиболее часто встречаемыми поражениями печени указаны в схеме №2 .
Схема №2

Медицинский туризм
Пройти лечение в Корее, Израиле, Германии, США
Медицинский туризм
Получить консультацию по медтуризму
Лечение
Цели лечения:
Замедление / прекращение прогрессирования заболевания печени;
Профилактика ЦП;
Профилактика ГЦК.
Тактика лечения
**
Достижение ответа на терапию. Выбор тактики ведения пациента с хроническим гепатитом В зависит от фазы вирусной инфекции и стадии заболевания печени: от динамического наблюдения и режимных (немедикаментозных) мероприятиях при неактивном носительстве HBsAg - до противовирусной терапии при активном гепатите.
Немедикаментозное лечение
Общие меры
:
Охранительный режим: избегать инсоляции, перегрева тела, в продвинутых стадиях заболевания и портальной гипертензии - ограничение физических нагрузок, облегчение режима работы (УД - В);
Барьерная контрацепция при половых контактах с не вакцинированными партнерами (УД - A);
Вакцинация против гепатита А (УД - A);
Вакцинация половых партнеров против гепатита В (УД -иA);
Индивидуальное пользование средствами личной гигиены (УД -A);
Минимизация факторов риска прогрессирования: исключение алкоголя, табака, марихуаны, гепатотоксичных лекарственных средств, включая биологически активные добавки, нормализация веса тела и т.д. (УД - A)
Медикаментозное лечение
Основу лечения хронического гепатита В составляет противовирусная терапия
(ПВТ) .
Общие показания к ПВТ :
HBV-ДНК ≥2 000 МЕ/мл
AЛТ ≥ верхней границы нормы (ВГН)
Тяжесть заболевания печени ≥ A2 и/или ≥ F2
Кроме того, учитываются возраст, общее состояние, семейный анамнез по ЦП, ГЦК, наличие внепеченочных проявлений и принадлежность пациентов к отдельным группам (Таблица №7).
Таблица №7
. Терапевтическая тактика в отдельных группах
|
Характеристика пациентов |
Тактика |
| Иммунотолерантная фаза |
HBeAg-позитивные пациенты < 30 лет с постоянно нормальной АЛТ высокой HBV DNA [обычно > 107 МЕ/мл], без признаков заболевания печени, без ГЦК и ЦП в семейном анамнезе не нуждаются в ПВТ Мониторинг каждые 3-6 месяцев У пациентов >30 лет и/или семейным анамнезом ГЦК - LBx и возможна ПВТ |
| HBeAg-негативные пациенты с нормальной АЛТ, HBV DNA 2000-20000 МЕ/мл |
Не нуждаются в срочной LBx и ПВТ Мониторинг АЛТ каждые 3 месяца HBV DNA - каждые 6-12 месяцев Через 3 года - мониторинг как при неактивном носительстве Непрямая эластография м.б. полезна |
| Активный ХГВ (HBeAg+/ HBeAg--) |
При АЛТ > 2ULN, HBV DNA > 20 000 МЕ/мл - ПВТ м.б. начата даже без LBx Непрямая эластография печени может быть полезна |
| Неактивные носители HBsAg |
В ПВТ не нуждаются Мониторинг каждые 6-12 месяцев |
| Компенсированный ЦП с HBV DNA (+) | . ПВТ в специализированный центрах даже при нормальной АЛТ |
| Декомпенсированный ЦП с HBV DNA (+) |
Неотложная ПВТ АН в специализированный центрах Определение показаний к ТП |
Для ПВТ ХГВ используются две стратегии :
. Длительное лечение аналогами нуклеотидов/нуклеозидов (данная стратегия направлена на поддержание ремиссии).
Перед проведением терапии пациенту должна быть предоставлена полная информация о терапии ПЕГ-ИФН и АН для совместного принятия решения о выборе метода лечения. Преимущества и недостатки стратегий ПВТ в зависимости от противовирусных агентов приведены в Таблице№8.
Таблица №8
. Преимущества и недостатки терапии на основе Пег-ИФН и АН
|
Препараты |
Преимущества | Недостатки |
| Пег-ИФН |
Отсутствие резистентности вируса Потенциальная возможность достижения иммунного контроля и устойчивого вирусологического ответа Высокая частота НВе- сероконверсии при 12-месячной терапии Вероятность клиренса / сероконверсии HBsAg у пациентов, достигших неопределяемый уровень HBV ДНК |
Риск побочных явлений Подкожное введение Противопоказания при декомпенсированном ЦП, аутоиммунных, психических и других сопутствующих заболеваниях, а также при беременности |
| АН |
Выраженный противовирусный эффект Возможность применения при беременности (Тенофовир, Телбивудин) |
Риск развития резистентности Неопределенная (во многих случаях - пожизненная) длительность терапии Отсутствие данных о безопасности длительного лечения |
Перечень противовирусных лекарственных средств, зарегистрированных в РК, представлен в Таблице №9.
Таблица№9
. Список лекарственных средств, одобренных для лечения ХГВ в РК и режим дозирования
|
МНН |
Фармакотерапевтическая группа | Форма выпуска | Режим дозирования |
| Пег-ИНФ альфа-2а |
Интерфероны Код АТХ L03АВ11 |
Раствор для инъекций 180 мкг/0,5 мл | 180 мкг еженедельно подкожно |
| Ламивудин |
Код ATС JO5AF05 |
100 мг в сутки внутрь | |
| Телбивудин |
Нуклеозиды - ингибиторы обратной транскриптазы Код АТX J05AF11 |
600 мг в сутки внутрь | |
| Тенофовир |
Нуклеозиды и нуклеотиды - ингибиторы обратной транскриптазы Код АТХ J05AF07 |
Таблетки, покрытые пленочной оболочкой, 300 мг | 300 мг в сутки внутрь |
| Энтекавир* |
Нуклеозиды-ингибиторы обратной транскриптазы Код АТX J05AF10 |
0,5 мг в сутки внутрь |
*Оригинальный препарат в РК не зарегистрирован
В качестве препаратов первой линии используются Пег-ИНФ альфа-2а или Тенофовир или Энтекавир, вызывающие наименьшую резистентность. Остальные АН можно применять для лечения ХГВ только при недоступности или невозможности использования АН первой линии.
В исследованиях было показано, что комбинация Пэг-ИФН и ламивудина не повышает достижение стойкого вирусологического или серологического ответа, комбинация с телбивудином характеризуется высоким риском тяжелой полинейропатии, а сведения об эффективности и безопасности комбинаций с тенофовиром и энтекавиром ограничены. Поэтому комбинации Пег-ИФН и АН не рекомендуются.
Основания для выбора режима терапии в отдельных клинических группах представлены в Таблице№10 .
Таблица №10
. Выбор режима терапии
| Предпочтительные препараты | |
| Пациенты молодого и среднего возраста без ЦП, женщины, желающие вылечиться перед беременностью | Пег-ИФН альфа-2а |
| Декомпенсированный ЦП | АН |
| Трансплантация печени | АН (Энтекавир, Тенофовир, Ламивудин) |
| Почечная недостаточность | Энтекавир |
| Беременность, женщины детородного возраста, планирующие беременность в ближайшее время | Тенофовир, Телбивудин |
| Паст-инфекция / оккультный гепатит до и вовремя проведения иммуносупрессивной терапии, химиотерапии | АН |
| ВГD | ПЕГ-ИФН альфа-2; в случае противопоказаний к ПЕГ-ИНФ альфа-2а или его неэффективности при наличии репликации HBV - АН |
| Коинфекция ВГС | ПЕГ-ИФН альфа-2 + RBV |
| ВИЧ-коинфекция | Тенофовир + Эмтрицитабин или Ламивудин |
Предикторы (факторы) ответа на ПВТ различиаются в зависимости от выбранной стратагии и противовирусного агента (Таблица №11). Учет этих факторов полезен для принятия решений о начале и продолжении противовирусной терапии .
Таблица №11 . Предикторы ответа на ПВТ
|
До начала ПВТ |
Во время ПВТ | |
| Пег-ИФН |
Высокая биохимическая активность (АЛТ > 2-5 ВГН) Высокая гистологическая активность (≥A2) Генотипы A и B HBV по сравнению с генотипами D и C Отсутствие ИФН-терапии в анамнезе |
При HBeAg-позитивном ХГВ HBe-сероконверсия ассоциирована со следующими факторами: Снижение ДНК HBV < 20 000 МЕ/мл через 12 недель (50%-й вероятность) Увеличение активности АЛТ после снижения уровня HBV ДНК Снижение уровня HBsAg < 1500 МЕ/мл через 12 недель Уровень HBeAg через 24 недели При HBeAg-негативном ХГВ стойкий ответ ассоциирован со следующими факторами: Снижение концентрации ДНК HBV < 20 000 МЕ/мл через 12 недель (50% вероятность) Снижение уровня HBsAg |
| АН |
При HBeAg-позитивном ХГВ HBe-сероконверсия ассоциирована со следующими факторами: Высокая активность АЛТ и высокая гистологическая активность |
Независимо от HBeAg-статуса низкий риск развития резистентности вируса, а также HBe-сероконверсия у HBeAg-позитивных пациентов ассоциированы со следующими факторами: Вирусологический ответа на 12 неделе Вирусологический ответ (неопределяемый уровень HBV ДНК) на 24 неделе |
Во время проведения ПВТ осуществляется стандартный мониторинг в целях оценки ее эффективности и безопасности (Таблица №12) .
Таблица №12 . Мониторинг ПВТ
| Исследования | Кратность | |
| Пег-ИФН | АН | |
| ОАК с подсчетом тромбоцитов | Каждые 2 недели в первый месяц, далее каждые 4 недели | Каждые 12 недель |
|
АЛТ, АСТ, Билирубин Альбумин, МНО |
Каждые 4 недели | Каждые 12 недель |
| Креатинин / клиренс креатинина, Мочевина | Каждые 12 недель | У пациентов с низким риском почечных осложнений* каждые 12 недель в первый год лечения, далее - каждые 24 недели при отсутствии ухудшения). У пациентов с высоким риском почечных осложнений* - каждые 4 недели в первые 3 месяца, далее каждые 12 недель до конца первого года лечения, далее - каждые 24 недели (при отсутствии ухудшения). При клиренсе креатинина менее 60 мл/мин или уровне фосфатов сыворотки менее 2 мг/дл целесообразна более частая оценка |
| Фосфаты | ||
|
ОАМ |
Каждые 12 недель | |
| ТТГ | Каждые 12 недель | |
| АФП | Каждые 24 недели у пациентов без ЦП, каждые 12 недель у пациентов с ЦП | |
| УЗИ ОБП | Каждые 24 недели у пациентов без ЦП, каждые 12 недель у пациентов с ЦП | Каждые 24 недели у пациентов без ЦП, каждые 12 недель у пациентов с ЦП |
| Осмотр глазного дна | Каждые 12 недель | |
| HBV DNA (качественный тест, при положительном результате - количественный | На 12, 24 и 48 неделях ПВТ и через 24 и 48 недель после ее окончания | Каждые 12 недель для подтверждения вирусологического ответа и далее каждые 12-24 недели во время ПВТ и после ее прекращения (при фиксированном курсе) |
| HBeAg / anti-HBe (у исходно HBeAg-позитивных пациентов) | На 24 и 48 неделях ПВТ и через 24 и 48 недель после ее окончания | Каждые 24 недели во время ПВТ и после ее прекращения (при фиксированном курсе) |
| HBsAg (количественный тест) | На 12 и 24 неделях ПВТ | |
| HBsAg (качественный тест) / anti-HBs | Каждые 48 недель после сероконверсии HBeAg и негативации HBV ДНК у HBeAg-позитивных пациентов или негативации HBV ДНК у HBeAg-негативных пациентов | Каждые 48 недель после сероконверсии HBeAg и негативации HBV ДНК у HBeAg-позитивных пациентов или негативации HBV ДНК у HBeAg-негативных пациентов во время ПВТ и после ее завершения (при фиксированном курсе) |
| Другие исследования (в зависимости от сопутствующих заболеваний и побочных явлений) | По показаниям | По показаниям |
*Декомпенсированный ЦП, клиренс креатинина менее 60 мл/мин, плохо контролируемая артериальная гипертензия, протеинурия, неконтролируемый сахарный диабет, активный гломерулонефрит, сопутствующая терапия нефротоксичными препаратами, трансплантация солидного органа
Виды ответа на ПВТ :
Биохимический ответ - нормализация АЛТ
Гистологический ответ - снижение ИГА ≥ 2 пунктов (HAI, Ishak) без прогрессирования фиброза
Серологический ответ (клиренс / сероконверсия HBsAg; клиренс / сероконверсия HBeAg у HBeAg-позитивных пациентов)
Вирусологический ответ отличается в зависимости от ПВТ (Таблица №13)
Таблица №13
. Виды вирусологического ответа
|
Препараты |
Виды вирусологического ответа | Определение |
| ПЕГ-ИФН | Вирусологический ответ | Концентрация HBV ДНК < 2000 МЕ/мл (оценивается на 6 месяце, в конце лечения, а также через 6 и 12 месяцев после окончания терапии) |
| Отсутствие вирусологического ответа | Концентрация HBV ДНК > 2000 МЕ/мл (оценивается на 6 месяце терапии, в конце лечения) | |
| Устойчивый вирусологический ответ | Уровень HBV ДНК < 2000 МЕ/мл спустя 12 месяцев после прекращения лечения | |
| Полный ответ | Устойчивый вирусологический ответ после ПВТ в сочетании с клиренсом HBsAg | |
| АН | Первичное отсутствие ответа | Снижение концентрации HBV ДНК < 1 log10 МЕ/мл от первоначального через 3 месяца после начала терапии; основная причина - резистентность |
| Вирусологический ответ | Отсутствие (неопределяемый уровень) HBV ДНК по данным высокочувствительной ПЦР (оценивается каждые 3-6 месяцев во время лечения) | |
| Снижение уровня ДНК HBV > 1 log10 МЕ/мл при наличии определяемой HBV ДНК через 6 месяцев после начала терапии | ||
| Вирусологический рецидив | Подтвержденное повышение уровня HBV ДНК > 1 log10 МЕ/мл по сравнению с наименьшим уровнем ДНК HBV, достигнутым на фоне лечения; основные причины - низкая приверженность к лечению и резистентность вируса | |
| Резистентность | Селекция мутантных штаммов HBV с заменами аминокислот в обратной транскриптазе, которые приводят к снижению чувствительности вируса к АН |
Конечные точки ПВТ :
Клиренс HBsAg (с формированием и без формирования anti-HBs) у HBeAg-позитивных и HBeAg-негативных пациентов;
Устойчивый вирусологический ответ (HBV DNA < 2000 МЕ/мл) и биохимический после ПВТ у HBeAg-негативных, а также исходно HBeAg-позитивных пациентов с устойчивой сероконверсией;
Вирусологическая ремиссия (сохраняющийся отрицательный результат HBV-ДНК при использовании чувствительной ПЦР) во время длительной ПВТ у HBeAg-позитивных пациентов, не достигших сероконверсии, а также у HBeAg-негативных пациентов
ПВТ на основе Пег-ИФН проводится фиксированным курсом (48 недель). ПВТ на основе АН также может проводится фиксированным курсом при достижении конечных точек (в основном, в случаях HBeAg-позитивного гепатита без ЦП). При отсутствии достижения конечных точек при НBeAg-позитивном гепатите, в большинстве случаев HBeAg-негативного гепатита, а также во всех случаях ЦП независимо от HBeAg-статуса, терапия АН проводится неопределенно долго (Таблица №14).
Таблица №14
. Длительность ПВТ в зависимости от режима и достижения конечных точек
| Препараты | HBeAg-позитивные пациенты | HBeAg-негативные пациенты | ||
| Конечные точки | Длительность / тактика ПВТ | Конечные точки | Длительность / тактика ПВТ | |
| Пег-ИФН* |
Стойкая сероконверсия HBeAg с одновременным снижением HBV ДНК< 2000 МЕ/мл и нормализацией АЛТ |
. 48 недель |
HBV ДНК < 2000 МЕ/мл (в идеале - неопределяемая HBV ДНК) В идеале - в сочетании с клиренсом / сероконверсией HBsAg |
. 48 недель |
| АН |
сероконверсия HBeAg с неопределяемой HBV ДНК и нормализацией АЛТ В идеале - в сочетании с клиренсом /сероконверсией HBsAg |
У пациентов без ЦП - 48 недель после сероконверсии HBeAg и неопределяемой HBV ДНК (стойкая сероконверсия сохраняется у 40-80% пациентов) |
. Клиренс / сероконверсия HBsAg с неопределяемой HBV ДНК и нормализацией АЛТ |
У пациентов без ЦП - до исчезновения HBsAg |
Неудачи терапии
Мониторинг терапии ХГВ, помимо достижения конечных точек, предусматривает определение промежуточных предикторов ее неэффективности, а также неудач, включая отсутствие ответа по окончании терапии и устойчивого вирусологического ответа (при фиксированных курсах), первичное отсутствие ответа, частичный вирусологический ответ и вирусологический прорыв (при длительных курсах) . Терапевтическая тактика в этих случаях представлена в Таблице №15.
Таблица №15 . Неудачи ПВТ и тактика при них
| Препараты |
Период |
Показатели неэффективности | Тактика | |
| HBeAg-позитивные пациенты | HBeAg-негативные пациенты | |||
| Пег-ИФН | 12 (24) неделя ПВТ | HBsAg > 20,000 МЕ/мл или не снижается и HBV ДНК не снижается или снижается менее чем на 2 log10 МЕ/мл | HBsAg не снижается и HBV ДНК не снижается или снижается менее чем на 2 log10 МЕ/мл | . Рассмотреть вопрос об отмене Пег-ИФН (особенно при генотипе D HBV) и назначении АН |
| 48 неделя (окончание) ПВТ и период последующего наблюдения | Определяется HBeAg или HBV ДНК > 2000 МЕ/мл | HBV ДНК > 2000 МЕ/мл | Рассмотреть вопрос о назначении АН | |
| АН | 12 неделя ПВТ | Первичное отсутствие ответа |
При отсутствии нарушений режима ПВТ желательно провести генотипирование штаммов HBV для выявления возможных мутаций Назначить АН с высоким генетическим барьером (тенфовир или энтекавир) в соответствии с профилем резистентности* |
|
| 24 неделя ПВТ | Частичный вирусологический ответ |
Оценить приверженность к терапии и правильность приема препарата Назначить АН с высоким генетическим барьером (тенофовир или энтекавир) в соответствии с профилем резистентности* |
||
| Любой период ПВТ | Вирусологический рецидив |
Оценить приверженность к терапии и правильность приема препарата (нарушения режима терапии особенно вероятны у пациентов, впервые получающих АН с высоким генетическим барьером - тенофовир или энтекавир) Назначить АН с высоким генетическим барьером в соответствии с профилем резистентности* При резистентности ко многим препаратам целесообразны генотипирование вируса и применение комбинации аналогов нуклеозидов и нуклеотидов (предпочтительно тенофовира) |
||
| Любой период после ПВТ (при ограниченном по времени курсе) | Рецидив | . Возобновить прием АН с высоким генетическим барьером (тенофовир или энтекавир) | ||
*в соответствии с Таблицей №16.
HBV склонен к спонтанным и медикаментозно-индуцированным мутациям - изменениям структуры ДНК в результате ошибок репликации, которые способствуют приобретению новых свойств. В результате некоторых мутаций формируется резистентность к лекарственным препаратам, что оказывает ключевое влияние на тактику ПВТ (Таблица №16) .
Таблица №16 . Резистентность на фоне терапии АН и тактика при ее развитии
|
Лекарственные препараты |
Риск развития резистентности | Тактика |
| Ламивудин (LAM) |
1 год - 24% 2 год - 38% 3 год - 49% 4 год - 67% 5 год - 70% |
Заменить на Тенофовир |
| Телбивудин (LdT) |
1 год - 4% 2 год - 17% |
|
| Энтекавир (ETV) |
1 год - 0,2% 2 год - 0,5% 3 год - 1,2% 4 год - 1,2% 5 год - 1,2% |
Заменить на Тенофовир или добавить Тенофовир |
| Тенофовир (TDF) | Не описана | Заменить на Энтекавир у пациентов, ранее не получавших Ламивудин, или добавить Энтекавир или Телбивудин или Ламивудин или Эмтрицитабин |
Пациенты с хронической HBV-инфекцией, включая тех, кому ПВТ не проводится, нуждаются в динамическом наблюдении в целях оценки прогрессирования заболевания и скрининга ГЦК. Кратность наблюдения и перечень обследования представлены в Таблице №17.
Таблица №17
. Динамическое наблюдение за пациентами с HBV-инфекцией
| Минимальный перечень исследований | Стадия заболевания | |
| F0-F3 | F4 | |
| Общий анализ крови с подсчетом тромбоцитов | Каждые 6 месяцев | Каждые 3 месяца |
| Функциональные пробы печени (АЛТ, АСТ, билирубин, креатинин, альбумин, МНО, щелочная фосфатаза) | Каждые 6 месяцев | Каждые 3 месяца |
| АФП | Каждые 6 месяцев | Каждые 3 месяца |
| УЗИ органов брюшной полости | Каждые 6 месяцев | Каждые 3 месяца |
| ПЦР: HBV ДНК (качественный тест, при положительном результате - количественный) | Каждые 6 месяцев | Каждые 3 месяца |
| anti-HDV | Каждые 6 месяцев | Каждые 6 месяцев |
| Другие исследования | Исследования, проводимые при ЦП по показаниям | |
Тактика в отдельных группах
Пациенты с суперинфекцией HDV
У всех пациентов с ХГВ должен проводиться скрининг на HDV (дельта)-инфекцию (определение anti-HDV)
При коинфекции HBV и HDV развивается острый гепатит, склонный с саморазрешению, но с более частыми фулминантными формами (по сравнению с моноинфекцией HBV)
При суперинфекции HDV чаще (до 90%) развивается хронический гепатит D, характеризующийся быстропрогрессирующим течением, высоким риском развития ЦП и ГЦК (4 и 2,8 % в год соответственно). Активная дельта-инфекция подтверждается наличием анти-HDV IgM и HDV РНК
Бессимптомные носители HDV с нормальной АЛТ, отсутствием гистологической активности и стадией заболевания < F2 нуждаются в мониторинге
ПВТ при ХГD проводится в соответствии со следующими положениями:
− Лечение показано пациентам с повышенной активностью трансаминаз и/или гистологической активностью, а также со стадией заболевания ≥ F2 по шкале METAVIR (согласно данным непрямой эластометрии или гистологического исследования), при этом лечение начинают как можно раньше
− Эффективность ПВТ может быть оценена на 3-6 месяце с помощью ПЦР, при этом отсутствие определяемого уровня HDV РНК на 6 месяце является прогностически благоприятным фактором достижения вирусологического ответа
− Имеются сведения о преимуществах пролонгации терапии свыше 1 года, однако, оптимальная длительность ПВТ до настоящего момента не определена
− У 25-30% пациентов по окончании лечения отмечается вирусологический ответ с неопределяемой HDV RNA и улучшением гистологии, а у некоторых - еще и потеря HBsAg, однако, во многих случаях наблюдается рецидив в первые 6 месяцев, а также в последующий период (поздний рецидив), в связи с чем термин «Устойчивый вирусологический ответ» не может использоваться применительно к HDV-инфекции
− В соответствии с результатами исследования HIDIT-2, у пациентов с ЦП вирусологический ответ выше, чем у пациентов без ЦП (51% vs 25%), при этом частота развития побочных явлений достоверно выше при ЦП
− В соответствии с результатами исследований HIDIT-1 и HIDIT-2, комбинация Пег-ИФН и АН не улучшает результаты терапии
− АН не влияют на репликацию HDV и ассоциированное заболевание. Тем не менее, терапия АН может быть рассмотрена у пациентов с активной репликацией HBV с постоянным или флюктуирующим уровнем HBV ДНК >2000 IU/ml (при ЦП - с определяемым уровнем HBV ДНК), особенно в случае неэффективности или невозможности применения Пег-ИФН.
Пациенты с коинфекцией HCV
У всех пациентов с ХГВ должен проводиться скрининг на ВГС (определение anti-HCV)
HCV - коинфекция ускоряет прогрессирование заболевания печени и повышает риск ГЦК
Уровень HBV ДНК чаще низкий или даже неопределяемый, а HCV вносит основной вклад в активность гепатита и прогрессирование заболевания
Показания к терапии ХГВ и ХГС определяются в соответствии со стандартными рекомендациями, однако, данная категория пациентов является приоритетной для инициации ПВТ
В случае реактивации HBV показана терапия АН.
Пациенты с коинфекцией ВИЧ
У всех пациентов с ХГВ должен проводиться скрининг на ВИЧ (anti-HIV)
У ВИЧ-инфицированных пациентов с ХГВ повышен риск ЦП и ГЦК
Антиретровирусная терапия может приводить к реактивации ХГВ в связи с восстановлением иммунного ответа
Показания к терапии ХГВ соответствуют таковым для пациентов без ВИЧ-инфекции
Большинство пациентов с коинфекцией ВИЧ нуждается в одновременном лечении обеих инфекций с использованием комбинации Тенофовира с Эмтрицитабином или Ламивудином в сочетании с третьим компонентом, активным в отношении ВИЧ (во избежание развития резистентности)
У некоторых пациентов с числом CD4 > 500/мкл можно рассмотреть вопрос лечения ХГВ до начала антиретровирусной терапии. При этом используются Пег-ИФН или Телбивудин, не активные против ВИЧ и не вызывающие развитие резистентности ВИЧ. В случае отсутствия достижения неопределяемого уровня HBV ДНК в течение 12 месяцев, назначают комбинированную терапию обеих инфекций, как указано выше.
Острый гепатит В
В некоторых случаях дифференцировать острый гепатит В от реактивации хронического гепатита крайне сложно и может потребоваться проведение гистологического исследования
Острый гепатит В склонен к саморазрешению с сероконверсией и формированием anti-HBs более чем у 95 % взрослых
При фулминантных формах показаны трансплантация печени и прием АН, при этом назначение Пег-ИФН противопоказано
Оптимальная длительность терапии АН не установлена, однако целесообразно продолжать ПВТ не менее 3 месяцев после HBsAg- сероконверсии или не менее 12 месяцев после HBeAg-сероконверсии без исчезновения HBsAg.
Профилактическое лечение при проведении иммуносупрессивной терапии
Во время иммуносупрессивной терапии (ИСТ), применяемой в лечении аутоиммуных и онкологических заболеваний, а также при проведении трансплантации костного мозга или солидных органов, имеется риск реактивации хронической HBV-инфекции
До начала ИСТ пациентам необходимо провести маркерную диагностику гепатита В
В случае положительных результатов на HBsAg и/или анти-HBc должны быть проведены следующие исследования:
− анти-HBs
− уровень ДНК HBV (качественный, количественный тесты)
− Функциональные пробы печени.
Тактика ведения пациентов в зависимости от результатов этих тестов представлена в Таблице №18.
Таблица №18
. Тактика профилактической ПВТ у пациентов, получающих ИСТ
|
HBsAg |
anti-HBc | anti-HBs |
HBV ДНК |
ИСТ | Тактика |
| + | > 2000 МЕ/мл | Тенофовир или энтекавир до начала ИСТ. ПВТ должна быть продолжена на протяжении 12 месяцев после достижения сероконверсии HBeAg и неопределяемого уровня HBV ДНК | |||
| + | > 2000 МЕ/мл | Продолжительность <6 мес. | Ламивудин до начала ИСТ. Контроль уровня HBV ДНК ежемесячно. Если ДНК HBV определяется после 3 мес. ПВТ, - заменить ламивудин на тенофовир. ПВТ нужно продолжать минимум 6 мес. после окончания ИСТ | ||
| Продолжительность >6 мес | Тенофовир или энтекавир до начала ИСТ. ПВТ нужно продолжать минимум 6 мес. после окончания ИСТ | ||||
| - | + | + или -- | Ритуксимаб или другая анти В-клеточная терапия | Ламивудин до начала ИСТ. ПВТ продолжить минимум 6 месяцев после окончания ИСТ | |
| + | + | -- | Не определяется | Мониторинг ДНК HBV ежемесячно. Если HBV ДНК начинает определяться, назначить АН и продолжить ПВТ минимум 6 мес. после окончания ИСТ | |
| < 2000 МЕ/мл | Не получают ритуксимаб или другую анти В-клеточную терапию, ИСТ менее 6 мес. | Ламивудин до начала ИСТ. Если через 6 мес. ПВТ продолжает определяться HBV ДНК, ламивудин заменить на тенофовир. ПВТ продолжить минимум 6 мес. после окончания ИСТ | |||
| > 2000 МЕ/мл | Не получают ритуксимаб или другую анти В-клеточную терапию, ИСТ более 6 мес. |
Энтекавир или тенофовир до начала ИСТ. ПВТ продолжить минимум 6 мес. после окончания ИСТ |
|||
| - | + | + | Не определяется | Не получают ритуксимаб или другую анти В-клеточную терапию | Профилактическая ПВТ не показана |
Кроме того, у HBsAg-негативных реципиентов печени от анти-HBc-позитивных доноров требуется профилактика АН (энтекавиром, тенофовиром, ламивудином), которая должна проводиться неопределенно долго.
Медицинские работники
В целях снижения риска передачи HBV-инфекции во время инвазивных процедур медицинским работникам может потребоваться ПВТ по особым показаниям
В случаях хронической HBV-инфекции с уровнем ДНК ≥ 2000 МЕ/мл целесообразна стандартная ПВТ
В случае применения АН предпочтительны препараты с высоким генетическим барьером (тенофовир или энтекавир), обеспечивающие достижение неопределяемого уровня HBV ДНК (в идеале) либо его снижение до менее чем 2000 МЕ/мл.
Планирование беременности и беременность
Медицинская помощь женщинам, планирующим беременность, а также беременным с хронической HBV-инфекцией, основывается на следующих общих положениях:
− Все женщины, обратившиеся в медицинские организации в связи с планированием беременности, а также при первом обращении для постановки на учет по беременности, в обязательном порядке подлежат обследованию на наличие HBsAg
− Беременные женщины, имеющие положительный результат скрининга на HBsAg, должны быть направлены на консультацию к гастроэнтерологу или инфекционисту, практикующим лечение вирусных гепатитов
− Оценка тяжести заболевания печени у беременных с хронической HBV-инфекцией соответствует таковой в общей популяции, за исключением проведения непрямой эластометрии
− Наличие хронической HBV-инфекции при компенсированном состоянии печени и отсутствии осложнений (гиперспленизм, варикозное расширение вен пищевода, желудка и другие признаки портальной гипертензии) не является противопоказанием для наступления беременности, естественного родоразрешения и кормления грудью
− Во время беременности следует проводить динамическое наблюдение за течением HBV-инфекции, включая регулярное (каждые 1-2 месяца) исследование общего анализа крови с подсчетом тромбоцитов и функциональных проб печени (АЛТ, АСТ, билирубин, альбумин, креатинин, МНО, щелочная фосфатаза), а также определение показателей, требуемых в случае назначения ПВТ
− Показания к ПВТ по поводу хронической HBV-инфекции у беременных, в целом, соответствуют таковым в общей популяции, однако, имеются противопоказания по применению ряда препаратов
− В конце 2 триместра беременности необходимо исследовать вирусную нагрузку для определения показаний к ПВТ в целях профилактики перинатальной трансмиссии
− Пег-ИФН абсолютно противопоказан, ламивудин и энтекавир по влиянию на беременность отнесены FDA к категории C, а тенофовир и телбивудин - к категории B (классификация основана на данных о тератогенности, полученных в доклинических исследованиях). При беременности предпочтительно использовать препараты категории В.
− До начала терапии HBV-инфекции следует обсудить вопросы планирования семьи, при этом женщина должна получить исчерпывающую информацию о безопасности и рисках препаратов в случае их приема во время беременности и кормления грудью
− Ребёнку, рождённому женщиной с HBV-инфекцией, в первые 8 часов после родов должна быть проведена активная (вакцина) и пассивная (HBIg) иммунизация против вирусного гепатита В в соответствии с инструкциями по применению зарегистрированных в РК препаратов
− У женщин с хронической HBV-инфекцией имеется риск реактивации гепатита в постнатальном периоде, особенно после отмены ранее назначенной ПВТ, в связи с чем таким женщинам целесообразно ежемесячное исследование функциональных проб печени как минимум на протяжении 6 месяцев после родов.
Женщины репродуктивного возраста с хронической HBV-инфекцией могут принадлежать к следующим группам:
− Женщины, планирующие беременность
− Беременные, не получающие ПВТ
− Женщины с беременностью, наступившей во время ПВТ
Тактика у женщин с хронической HBV-инфекцией, планирующих беременность, заключается в следующем:
− При отсутствии показаний к противовирусной терапии пациентка подлежит динамическому наблюдению
− В случае отсутствия активного заболевания печени и стадии менее F3 возможна отсрочка терапии до рождения ребенка
− При наличии активного заболевания печени со стадией F3 и выше (тяжелом фиброзе и циррозе) у женщин, которые согласны отложить запланированную беременность, целесообразно провести курсовое лечение Пег-ИФН, при этом следует помнить о необходимости эффективной контрацепции во время лечения. В случае невозможности или неэффективности терапии Пег-ИФН, а также в случае планирования беременности в ближайшее время, показана терапия АН, которую рекомендуется продолжать во время наступившей беременности и после нее, при этом тенофовир представляется наиболее рациональным выбором
Тактика у беременных с хронической HBV-инфекцией, не получавших ПВТ, заключается в следующем:
− При отсутствии показаний к противовирусной терапии и вирусной нагрузке HBV ДНК менее 1 000 000 МЕ/мл пациентка подлежит динамическому наблюдению
− В случае стадии заболевания печени менее F3 и вирусной нагрузке HBV ДНК менее 1 000 000 МЕ/мл возможна отсрочка терапии до рождения ребенка
− В случае отсутствия активного заболевания печени, стадии менее F3 и высокой вирусной нагрузке HBV ДНК (1 000 000 МЕ/мл и выше), особенно при HBeAg-позитивном статусе, имеется высокий риск вертикального заражения (10%), несмотря на активную и пассивную иммунизацию ребенка. Таким женщинам в целях профилактики перинатальной трансмиссии в течение всего 3 триместра назначают АН (тенофовир или телбивудин или ламивудин). Контрольное определение HBV ДНК проводят через 8 недель, а прием препаратов рекомендуют продолжить в течение 12 недель после родов. В дальнейшем необходимость в ПВТ определяется по общим показаниям
− В случае наличия активного заболевания печени с тяжелым фиброзом или циррозом показана стандартная ПВТ с использованием препаратов категории В, из которых наиболее предпочтителен тенофовир. По общим показаниям терапию продолжают после родов
Тактика у женщин с беременностью, наступившей во время ПВТ по поводу ХГВ, заключается в следующем:
− В случаях, когда пациентка во время беременности продолжает принимать назначенные ранее противовирусные препараты, показания к терапии HBV-инфекции должны быть пересмотрены
− В случае отсутствия тяжелого фиброза или цирроза и вирусной нагрузки HBV ДНК менее 1 000 000 МЕ/мл строгих показаний для продолжения противовирусной терапии нет и пациентка подлежит динамическому наблюдению
− В случае применения у пациентки с тяжелым фиброзом или циррозом печени противовирусных препаратов, относящихся к категории В, терапия ими должна быть продолжена во время беременности и по общим показаниям - после родов
− В случае применения при тяжелом фиброзе или циррозе печени противовирусных препаратов, противопоказанных при беременности, пациентку следует проинформировать о возможных рисках влияния данных препаратов на плод. В дальнейшем при сохранении беременности их следует заменить на препараты категории В, из которых предпочтителен тенофовир в связи с его большей активностью, высоким порогом резистентности и доступной информацией по безопасности у беременных женщин. По общим показаниям терапию продолжают после родов.
Реципиенты почки и пациенты на гемодиализе
Все реципиенты почки и пациенты на гемодиализе подлежат обязательному исследованию на наличие HBsAg
Серонегативным пациентам (с отрицательными результатами маркерной диагностики) требуется вакцинация против вирусного гепатита В
Пациентам с хронической болезнью почек, имеющим ХГВ, возможно проведение ПВТ с использованием Пег-ИФН и АН, при этом необходима коррекция доз препаратов в соответствии с инструкцией по применению
У пациентов, перенесших трансплантацию почки, Пег-ИФН противопоказан и проведение ПВТ возможно только с использованием АН. Данная терапия должна быть назначена даже при отсутствии активного заболевания печени всем HBsAg-позитивным реципиентам, получающим ИСТ, в целях профилактики реактивации HBV-инфекции
Во время ПВТ необходим регулярный мониторинг функции почек для своевременной коррекции режима терапии.
Пациенты с циррозом печени
Каждому пациенту с ЦП в исходе ХГВ определяются показания к ТП на основе стандартных оценочных шкал (CTP, MELD)
При компенсированном ЦП в исходе ХГВ ПВТ проводится независимо от вирусной нагрузки в стандартном режиме с использованием Пег-ИФН и АН
При декомпенсированном ЦП в исходе ХГВ Пег-ИФН противопоказан. ПВТ проводится АН, назначаемыми независимо от вирусной нагрузки, при этом следует иметь ввиду риск развития лактат-ацидоза (особенно на фоне терапии энтекавиром), что требует проведения тщательного клинико-лабораторного мониторинга
ПВТ на основе АН при ЦП назначается на длительный период времени с регулярным (каждые 3 месяца) мониторинге HBV ДНК для своевременной коррекции терапии в случае ее неудачи
В лечении ЦП среди АН предпочтительны тенофовир и энтекавир в виде монотерапии в связи с их высокой противовирусной активностью и минимальным риском резистентности; у пациентов с клиренсом креатинина менее 50 мл/мин дозы АН должны быть снижены в соответствии с инструкцией по применению
Всем пациентам с ЦП, независимо от статуса терапии и ее эффективности, включая случаи достижения устойчивого вирусологического ответа и вирусологической ремиссии, обязателен регулярный (1 раз в 3 месяца) скрининг на ГЦК, с учетом существующего риска.
Пациенты после ТП по поводу HBV-ассоциированных заболеваний печени
Всем пациентам с планируемой ТП по поводу HBV-ассоциированных заболеваний печени в до- и посттрансплантационном периоде требуется ПВТ с использованием АН, предпочтительно, 1 линии
(менее 100% вероятности применения):
|
МНН |
Форма выпуска |
| Ламивудин | Таблетки, покрытые пленочной оболочкой, 100 мг |
| Телбивудин | Таблетки, покрытые пленочной оболочкой, 600 мг |
| Энтекавир | Таблетки диспергируемые 0,5 мг |
| Эпоэтин альфа | |
| Эпоэтин бета | 2000 МЕ 15 |
| Филграстим | 30 млн.ЕД |
| Парацетамол | таблетки 500 мг |
| Левотироксин натрия | таблетки 25 мкг |
| Левотироксин натрия | |
| Ламивудин | Таблетки, покрытые пленочной оболочкой, 100 мг |
| Телбивудин | Таблетки, покрытые пленочной оболочкой, 600 мг |
| Энтекавир | Таблетки диспергируемые 0,5 мг |
| Эпоэтин альфа | раствор для инъекций в готовых к употреблению шприцах 2000 МЕ/0,5 мл 15 |
| Эпоэтин бета | 2000 МЕ 15 |
| Филграстим | 30 млн.ЕД |
| Парацетамол | таблетки 500 мг |
| Левотироксин натрия | таблетки 25 мкг |
| Левотироксин натрия | таблетки 50 мкг |
| Левотироксин натрия | таблетки 50 мкг |
| Адаметионин | лиофилизированный порошок, 500 мг |
| Тромбоконцентрат | в/в |
Медикаментозное лечение, оказываемое на этапе скорой неотложной помощи: нет.
Другие виды лечения: нет.
Хирургическое вмешательство: нет.
Профилактические мероприятия:
Обязательная вакцинация против гепатита В всем новорожденным и декретированным группам
Ранняя вакцинация новорожденных от HBsAg-позитивных матерей вакциной против гепатита В и иммуноглобулином человека против гепатита В (HBIG) в соответствии с инструкциями зарегистрированных в РК препаратов
Использование барьерных контрацептивов (презервативов) при контактах HBsAg - позитивных лиц с сексуальными партнерами, не имеющих HBV-инфекции, постинфекционного либо поствакцинального иммунитета.
Показания для плановой госпитализации:
Выраженная активность заболевания;
Декомпенсация заболевания печени (включая осложнения цирроза печени в исходе хронического вирусного гепатита В);
Пункционная биопсия печени;
Начальный период противовирусной терапии у пациентов с прогнозируемыми побочными явлениями средней и тяжелой степени;
Побочные явления в результате противовирусной терапии (цитопении, инфекции, психоневрологические нарушения и другие побочные явления средней и тяжелой степени);
Определение показаний и обследование перед трансплантацией печени.
Информация
Источники и литература
- Протоколы заседаний Экспертного совета РЦРЗ МЗСР РК, 2015
- 1. EASL Clinical Practice Guidelines: Management of chronic hepatitis B virus infection. Journal of Hepatology, 2012 vol. 57 p. 167–185. 2. NICE clinical guideline: Diagnosis and management of chronic hepatitis B in children, young people and adults//June 2013. 3. The Korean Association for the Study of the Liver (KASL) Clinical Practice Guidelines: Management of chronic hepatitis B. Clin Mol Hepatol Volume_18 Number_2 June 2012. 4. Sherlock"s Diseases of the Liver and Biliary System 12th Edition by James S. Dooley (Editor), Anna Lok (Editor), Andrew K. Burroughs (Editor), Jenny Heathcote (Editor), 2011. 5. Management of chronic hepatitis B: Canadian Association for the Study of the Liver consensus guidelines, Carla S Coffin MD MSc, FRCPC, Scott K Fung MD, FRCPC, Mang M Ma MD, FRCPC, Can J Gastroenterol Vol 26 No 12, December 2012. 6. American Association for the Study of Liver Diseases: Liver Biopsy, Don C. Rockey, Stephen H. Caldwell, Zachary D. Goodman, Rendon C. Nelson, and Alastair D. Smith. Hepatology, March 2009. 7. Noninvasive models of liver fibrosis, Zeng et al. Croat Med J. 2015;56:272-9 doi: 10.3325/cmj.2015.56.272. 8. EASL-ALEH Clinical Practice Guidelines: Non-invasive tests for evaluation of liver disease severity and prognosis. J.Hepatol (2015), http://dx.doi.org/10.1016/j.jhep.2015.04.006. 9. Wong GL, Wong VW, Choi PC, Chan AW, Chan HL. Development of a noninvasive algorithm with transient elastography (Fibroscan) and serum test formula for advanced liver fibrosis in chronic hepatitis B. Aliment Pharmacol Ther 2010;31:1095–1103. 10. Wong GL, Chan HL, Choi PC, Chan AW, Yu Z, Lai JW, et al. Non-invasive algorithm of enhanced liver fibrosis and liver stiffness measurement with transient elastography for advanced liver fibrosis in chronic hepatitis B. Aliment Pharmacol Ther 2014;39:197–208. 11. Comparison of Diagnostic Accuracy of Aspartate Aminotransferase to Platelet Ratio Index and Fibrosis-4 Index for Detecting Liver Fibrosis in Adult Patients With Chronic Hepatitis B Virus Infection: A Systemic Review and Meta-analysis, Xiao et al. Hepatology, January 2015. 12. Kim HC, Nam CM, Jee SH, Han KH, Oh DK, Suh I. Normal serum aminotransferase concentration and risk of mortality from liver diseases: prospective cohort study. BMJ 2004;328:983. 13. Prati D, Taioli E, Zanella A, Della Torre E, Butelli S, Del Vecchio E, et al. Updated definitions of healthy ranges for serum alanine aminotransferase levels. Ann Intern Med 2002;137:1-10. 14. Kariv R, Leshno M, Beth-Or A, Strul H, Blendis L, Kokia E, et al. Reevaluation of serum alanine aminotransferase upper normal limit and its modulating factors in a large-scale population study. Liver Int 2006;26:445-450. 15. Polish HBV Expert Group, Therapeutic recommendations for 2013: antiviral treatment for chronic hepatitis B. Przegl epidemiol 2013; 67: 287 – 295. 16. Kao JH, Wu NH, Chen PJ, Lai MY, Chen DS. Hepatitis B genotypes and the response to interferon therapy. J Hepatol 2000;33:998-1002. 17. Keeffe EB, Dieterich DT, Han SH, Jacobson IM, Martin P, Schiff ER, et al. A treatment algorithm for the management of chronic hepatitis B virus infection in the United States: 2008 update. Clin Gastroenterol Hepatol 2008;6:1315-1341. 18. Wedemeyer H, Yurdaydin C, Dalekos GN, Erhardt A, Cakaloglu Y, Degertekin H, et al. Peginterferon plus adefovir versus either drug alone for hepatitis delta. N Engl J Med 2011;364:322–331. 19. Yurdaydin C, Idilman R, Bozkaya H, Bozdayi AM. Natural history and treatment of chronic delta hepatitis. J Viral Hepat 2010;17:749–75. 20. Papatheodoridis GV, Manolakopoulos S, Touloumi G, Vourli G, Raptopoulou-Gigi M, Vafiadis-Zoumbouli I, et al. Virological suppression does not prevent the development of hepatocellular carcinoma in HBeAg-negative chronic hepatitis B patients with cirrhosis receiving oral antiviral(s) starting with lamivudine monotherapy: results of the nationwide HEPNET. Greece cohort study. Gut 2011;60:1109–1116. 21. Gunson RN, Shouval D, Roggendorf M, Zaaijer H, Nicholas H, Holzmann H, et al. Hepatitis B virus (HBV) and hepatitis C virus (HCV) infections in health care workers (HCWs): guidelines for prevention of transmission of HBV and HCV from HCW to patients. J Clin Virol 2003;27:213–230. 22. Bzowej NH, Hepatitis B. Therapy in pregnancy. Curr Hepat Rep 2010;9:197–204. 23. Xu WM, Cui YT, Wang L, Yang H, Liang ZQ, Li XM, et al. Lamivudine in late pregnancy to prevent perinatal transmission of hepatitis B virus infection: a multicentre, randomized, double-blind, placebo-controlled study. J Viral Hepat 2009;16:94–103. 24. Han GR, Cao MK, Zhao W, Jiang HX, Wang CM, Bai SF, et al. A prospective and open-label study for the efficacy and safety of telbivudine in pregnancy for the prevention of perinatal transmission of hepatitis B virus infection. J Hepatol 2011;55:1215–1221.
Информация
III. ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Нерсесов Александр Витальевич - доктор медицинских наук, профессор, заведующий кафедрой гастроэнтерологии и гепатологии с курсом эндоскопии, руководитель отдела гастроэнтерологии и гепатологии РГП на ПХВ «Научно - исследовательский институт кардиологии и внутренних болезней», Председатель Казахской Ассоциации по изучению печени, член Европейской, Американской, Азиатско-Тихоокеанской Ассоциации по изучению печени, Японского общества гепатологов
2) Калиаскарова Кульпаш Сагындыковна - доктор медицинских наук, профессор кафедры АО «Медицинский университет Астана», главный внештатный гастроэнтеролог МЗСР РК.
3) Доскожаева Сауле Темирбулатовна - доктор медицинских наук, профессор АО «Казахский медицинский университет непрерывного образования», проректор по учебной и научной работе, заведующая кафедрой инфекционных болезней.
5) Конысбекова Алия Анапьяровна - гастроэнтеролог, АО «Республиканский диагностический центр».
6) Калиева Мира Маратовна - клинический фармаколог, доцент кафедры клинической фармакологии и фармакотерапии РГП на ПХВ «Казахский национальный медицинский университет имени С.Д Асфендиярова».
Указание на отсутствие конфликта интересов:
нет.
Рецензенты:
1. Маевская Марина Викторовна - доктор медицинских наук, заведующая отделением гепатологии, Клиники пропедевтики внутренних имени В.Х. Василенко Первого Московского медицинского университета имени И.М. Сеченова, Вице президент российского общества по изучению печени.
2. Кошерова Бахыт Нургалиевна - доктор медицинских наук, профессор, проректор по клинической работе и НПР РГП на ПХВ «Карагандинский государственный медицинский университет»:
3. Рахметова Венера Саметовна -доктор медицинских наук, руководитель отдела гепатологии, АО «Национальный научный медицинский центр»
Прием предложений (с заполненной формой обоснования) идет до 29 марта 2019 года: [email protected] , [email protected] , [email protected]
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement, не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement является исключительно информационно-справочным ресурсом. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.
По определению ВОЗ, хронический гепатит (ХГ) — это хронический воспалительный процесс в печени, который длится на протяжении 6 месяцев и дольше. Хронический гепатит — это хронический рецидивирующий диффузный деструктивно-воспалительный процесс, морфологически характеризующийся персистенцией некрозов, воспалением, фиброзом при сохранении общей архитектоники печени.
Хронический вирусный гепатит В (ХВГВ) — прогрессирующее заболевание печени, вызванное вирусом гепатита В (HBV), одна из актуальных проблем медицины в связи с непрерывно увеличивающейся заболеваемостью, частым развитием неблагоприятных исходов (цирроз печени, гепатокарцинома) и высокой летальностью. По данным ВОЗ, 7% населения земного шара (более 400 млн чел.) являются носителями HBV.
HBV имеет высокую генетическую вариабельность из-за наличия этапа транскрипции в репликации с образованием прегенома. Чаще мутации происходят в участке гена, кодирующего синтез HBeAg. Замена гуанина на аденин в pre-core зоне HBV вызывает формирование участка ДНК, препятствующего считыванию информации и синтезу HBeAg. Мутировавший вирус «HBV минус HBeAg» ускользает от иммунной защиты, длительно сохраняется в организме, избегая элиминации. Мутации HBV приводят к повышению его патогенности и более тяжелому течению заболевания. В сыворотке крови одновременно с HBsAg выявляются ДИК-HBV. Мутантные штаммы HBV имеют особенный профиль серологических маркеров инфицирования (HBsAg при отсутствии анти-НВс, HBeAg и анти-НВе), полимеразная цепная реакция (ПЦР) определяет наличие ДНК-HBV.
В течении хронического вирусного гепатита B выделяют две фазы — репликативную и интегративную. В репликативной фазе происходит репликация ДНК-HBV и синтез HBcAg, HBeAg и HBsAg. Она определяет тяжесть поражения и контагиозность больных. Внепеченочная репликация приводит к генерализованной вирусной инфекции, системным проявлениям заболевания. В интегративной фазе происходит интеграция ДНК-HBV в геном гепатоцитов, в неактивном состоянии вирус сохраняется в ядрах. В этой фазе в крови отсутствуют ДHK-HBV, ДНК-полимераза, HBeAg, определяются анти-НВе (сероконверсия HBeAg в анти-НВе), HBsAg, могут быть выявлены антитела IgG к НВс.
При гепатитах наиболее важный диагностический и прогностический критерий — некроз паренхимы печени. Однако имеются две существенные особенности. Первая — в печеночной ткани отсутствуют некротизированные гепатоциты, а видны лишь участки печеночной дольки, замещенные мононуклеарными инфильтратами. Вторая — отсутствие полиморфноядерных лейкоцитов, стереотипной реакции на некроз во всех органах и тканях. Следовательно, основным механизмом гибели гепатоцитов при хронических поражениях печени, в том числе и при HBV-инфекции, является апоптоз. Характерным гистологическим признаком вирусного гепатита являются округлые гомогенные эозинофильные образования, часто содержащие пикнотические ядра. Гепатоциты в состоянии апоптоза называются тельцами Каунсильмена. В клетках в состоянии апоптоза, который является защитным механизмом, не происходит вирусной репликации.
Хронический вирусный гепатит В чаще имеет малосимптомное сглаженное течение. У большинства больных в течение 5-10 лет после инфицирования клинические симптомы отсутствуют. Первым в дебюте клинической картины чаще проявляется астеновегетативный синдром .Больные жалуются на слабость, быструю утомляемость, чувство усталости после ночного сна, головную боль, нервозность. Позднее возникают диспепсические расстройства. Появляются тяжесть в эпигастральной и правой подреберной областях, тошнота, горечь во рту, снижается аппетит. Важным объективным клиническим симптомом болезни является гепатомегалия . Край печени при пальпации часто болезненный, умеренно плотный, гладкий. Такое малосимптомное течение на протяжении длительного периода наблюдается у 65-70% больных с ХВГВ. У 30-35% заболевание протекает с более выраженной клинической картиной с ремиссиями и обострениями. Нередко появляются внепеченочные знаки. К ним относят телеангиэктазии, пальмарную и плантарную эритемы.
HBV может вызывать полиорганное поражение с разнообразными внепеченочными (системными) проявлениями. Выделяют две группы патогенетических механизмов их развития. К первой относят патологические изменения, развивающиеся в результате преимущественно реакций гиперчувствительности замедленного типа — миокардит, перикардит, артриты, миозиты, поражение легких (гранулематозы), синдром Шегрена. Вторая группа внепеченочных проявлений включает патологию, возникающую преимущественно вследствие иммунокомплексных реакций с повреждающим действием на стенки сосудов и развитием васкулитов. К клиническим вариантам внепеченочных проявлений при HBV-инфекции, связанных с образованием в тканях иммунных комплексов (ИК), относят: гломерулонефриты; артриты; ревматические полимиалгии; вторичные смешанные криоглобулинемии; папулезные акродерматиты.
Диагноз хронический вирусный гепатит В устанавливают при наличии клинико-лабораторной симптоматики хронического гепатита (гепатомегалия, спленомегалия, синдром цитолиза, холестаза, мезенхимальный воспалительный синдром) с использованием серологических маркеров HBV -инфекции и результатов ПЦР. По результатам пункционной биопсии печени проводят морфологическую верификацию диагноза.
Лабораторную диагностику следует проводить поэтапно, от простых методов, доступных всем лечебным учреждениям, к более сложным, выполняемым в крупных специализированных центрах (см. табл. 1).
|
Этап |
Метод |
|
Первичная неспецифическая диагностика хронических диффузный поражений печени |
Биохимические исследования; |
|
Серологические методы; |
|
|
Определение стадии фиброза печени |
|
|
Обследование для решения вопроса о возможности проведения противовирусной терапии (ПВТ) |
Исследование щитовидной железы. |
Первичная неспецифическая диагностика хронических диффузных поражений печени
Первичная диагностика начинается с общего анализа крови, мочи и исследования основных биохимических показателей.
В гемограмме убольшинства пациентов изменения отсутствуют, реже определяют умеренную анемию, лейкопению, нейтропению, лимфопению, тромбоцитопению, увеличение СОЭ. Чаще изменения в анализах крови обусловлены действием вируса на костный мозг.
На первом этапе диагностики определяют следующие биохимические показатели: уровни аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), щелочной фосфатазы (ЩФ), гамма-глутамилтранспептидазы (ГГТП), альбуминов, холинэстеразы, билирубина и его фракции, протромбиновый индекс, тимоловую пробу (ТП). АЛТ локализуется в основном в цитозольной фракции гепатоцитов. При нарушении внутренней структуры этих клеток и повышении их проницаемости фермент попадает в кровь в большей концентрации, что характерно как для острого гепатита, так и для обострения хронического. АЛТ считается индикаторным ферментом, который является основным показателем в лабораторном синдроме цитолиза. При заболеваниях печени АЛТ повышается раньше и в большей степени, чем ACT. ACT находится преимущественно в митохондриях гепатоцитов (80%), проникает в кровь при более тяжелых повреждениях этих клеток. АЛТ считается более чувствительным ферментом в ранней диагностике поражений печени по сравнению с ACT.
При умеренном воспалительном процессе в печени митохондрии повреждаются незначительно. В кровь полностью высвобождаются АЛТ, содержащаяся в цитозоле, и меньшая фракция ACT. Коэффициент де Ритиса (соотношение АСТ/АЛТ при вирусных гепатитах <1,33 ед (чаще 0,6-0,8 ед). При тяжелом течении гепатитов в кровь поступает основная (митохондриальная) фракция ACT из гепатоцитов. В этих случаях показатели ACT приобретают особую диагностическую и прогностическую значимость. Необходимо помнить, что резкое повышение ACT характерно для поражений сердечной мышцы (чаще при инфаркте миокарда), коэффициент де Ритиса >1,33.
Общий билирубин, неконъюгированный (непрямой) и конъюгированный (прямой). При диффузных поражениях печени с развитием паренхиматозной желтухи прямой билирубин не экскретируется в желчные капилляры, содержание его в крови значительно возрастает. Прямой билирубин может фильтроваться в почках и накапливаться в моче (в отличие от непрямого билирубина). Количество непрямого билирубина в крови также увеличивается из-за нарушения синтеза гепатоцитами билирубин-глюкуронидов. Прогрессирующее повышение концентрации свободного билирубина свидетельствует о тяжелом поражении печеночной ткани и считается прогностически неблагоприятным. Уровень билирубинемии зависит также от темпов прогрессирования заболевания, может быть признаком печеночной недостаточности.
Щелочная фосфотаза в печени локализуется в микроворсинках желчных канальцев, в меньшей степени в цитозоле гепатоцитов. Повышение уровня этого фермента в крови свидетельствует о наличии холестаза (как внутри-, так и внепеченочного).
Гамма-глутамилтранспептидаза более чувствительна при повреждении гепатоцитов, чем АЛТ и АСТ, считается органоспецифическим ферментом, индикаторным показателем гепатоксичности. Причинами повышения ГГТП в крови чаще всего являются: холестаз, цитолиз, алкогольная и лекарственная интоксикация, неопластический процесс в печени. Динамика активности ГГТП дает возможность проводить контроль эффективности лечения.
Альбумины сыворотки, холинэстеразу и протромбиновый индекс относят к индикаторам гепатодепрессивного (гепатопривного) синдрома или синдрома малой печеночной недостаточности, который предусматривает любые нарушения метаболической функции печени без энцефалопатии.
Определение холинэстеразы , альбуминов и протромбинового индекса считают пробами средней чувствительности. Снижение показателей этих индикаторов гепатодепрессии средней чувствительности на 10-20% расценивают как незначительное, на 21-40% — как умеренное, более чем на 40% — как значительное.
Тимоловую пробу относят к индикаторам мезенхимально-воспалительного синдрома. Повышение ТП отражает изменение коллоидной устойчивости сыворотки крови, вызванное уменьшением соотношения альбумины/глобулины, увеличением содержания глобулиновых фракций. Печень — основной, но не единственный, белковосинтезирующий орган. Поэтому повышение ТП можно наблюдать при всех заболеваниях, сопровождающихся диспротеинемией. Длительное и значительное повышение показателей ТП может быть обусловлено переходом острого гепатита в хронический и указывать на активность процесса.
УЗИ — этап первичной диагностики диффузных изменений печени. При ХВГВ определяют умеренно выраженную гепатомегалию без деформации контуров. Структура печени чаще однородная, эхогенность может быть умеренно и равномерно повышена, возможно утолщение капсулы (норма до 3 мм).
Признаки портальной гипертензии отсутствуют (диаметр портальной вены меньше 13 мм, селезеночной — меньше 6,2 мм). Может наблюдаться умеренное увеличение селезенки.
Специфическая диагностика HBV-инфекции
Специфическая диагностика HBV -инфекции начинается с использования серологических методов: иммуноферментного анализа (ИФА) с диагностикумами ELISA III поколения и иммунохроматографического анализа (ИХА). Последний является методом экспресс-диагностики. ИФА-диагностикумы высокочувствительны (не менее 96%) и специфичны (не менее 98%). Недостаток метода в длительности исследования (минимум несколько часов) — в большинстве лабораторий результат может быть получен не раньше чем через 24 ч. Существенной является и высокая стоимость исследования.
В последнее время для диагностики вирусных гепатитов используют экспресс-методы, которые удобны в работе поликлиник. Преимущества их следующие: быстрота (ответ может быть получен через 15 мин), достаточная точность, возможность проведения анализа каждому больному в момент сдачи крови (без накопления определенного количества образцов). Используются тестовые полоски, панели или тест-кассеты, которые обеспечивают быстроту получения результата. Экспресс-диагностика основана на методе ИХА (стрип-тест, Quik Strip cassete), который позволяет в биологических жидкостях (цельная кровь, сыворотка, слюна, моча, кал) выявить определенные концентрации маркеров HBV. Чувствительность и специфичность этих тестов полностью сопоставимы с таковыми метода ИФА. Экспресс-тесты удобны в использовании, дают возможность немедленно уточнить диагноз во многих сложных ситуациях. Например, определить профиль отделения для госпитализации пациента с желтухой, необходимость срочного оперативного вмешательства или переливание крови непосредственно от донора.
ИФА или экспресс-методы позволяют определить наличие диагностических маркеров HBV (маркеры инфицирования). Это антигены и антитела, выявление которых дает возможность установить наличие вируса, характеризовать течение инфекции, прогнозировать ее исход оценить эффективность лечения, судить о предыдущем контакте с вирусом, вызвавшим гепатит, а также о поствакцинальном иммунитете. При HBV-инфекции возможно выявление следующих маркеров.
Поверхностный антиген (HBsAg ) — определяется при острой или хронической HBV-инфекции. Обнаруживается на 3-5-й неделе от момента инфицирования. Продолжительность циркуляции антигена в среднем 70-80 дней от начала желтушного периода. Быстрое исчезновение (в первые дни желтушного периода) HBsAg с появлением анти- HBs класса IgM служит прогностически неблагоприятным признаком, свидетельствующим о возможном развитии фульминантного гепатита. Элиминация HBsAg и появление антител к нему — это непременное условие выздоровления. Анти- HBs в сыворотке крови обнаруживают не сразу после исчезновения HBsAg . Период, в течение которого не удается определить ни HBsAg , ни анти- HBs , называется фазой окна (window period ) . В это время единственным маркером, выявляемым в сыворотке крови, может быть анти- HBclgM . Время первого выявления анти- HBs после исчезновения HBsAg варьирует от 3-4 недель до 1 года (чаще через 3 мес).
Анти- HBslgG ретроспективно подтверждают ранее перенесенную HBV-инфекцию, характеризуют развитие постинфекционного иммунитета, позволяют оценивать напряженность поствакцинального иммунитета. Общие антитела к ядерному антигену HBV (анти-НВс ) определяют только для ретроспективной диагностики гепатита В, которые включают как IgM , так и IgG к HBcAg и не позволяют судить об острой либо перенесенной инфекции. анти- HBclgM появляются в крови через 1-2 нед после первичного обнаружения HBsAg у 4-20% больных с острым вирусным гепатитом В (ОВГВ) и являются единственным серологическим маркером в период «окна». Определяются они в течение 2-18 мес. Наличие анти- HBclgM в большинстве случаев свидетельствует об острой инфекции или о ХВГВ с продолжающейся репликацией HBV . Анти- HBclgM определяют при диагностике острого периода и реконвалесценции ОВГВ, хронического носительства HBV , ХВГВ с наличием анти- HBs . Анти- HBclgG появляются позднее а нти- HBclgM и могут определяться в течение многих лет. Они указывают на перенесенный, разрешившийся полностью гепатит либо на персистенцию HBV .
HBeAg появляется на ранних стадиях ОВГВ через небольшой промежуток времени после HBsAg и к началу развернутой картины уже не определяется. Одновременное длительное определение HBeAg и HBsAg характерно для перехода в хроническую форму ВГВ. Наличие HBeAg характеризует репликацию HBV высокую инфекционность крови, контагиозность больного, значительную активность воспалительного процесса. Для активной репликации вируса характерно наличие HBeAg и ДНК HBV . HBeAg циркулирует в крови только в присутствии HBsAg . В течение 1 -й недели желтушного периода HBeAg обнаруживают одновременно или через неделю после выявления HBsAg у 85-95% больных. Длительность циркуляции HBeAg имеет важное прогностическое значение. В большинстве случаев ОВГВ на протяжении 8 нед происходит сероконверсия от HBeAg к анти-НВе , прогноз считается благоприятным. Примерно у 10% пациентов к концу 9-й недели острого периода заболевания продолжают обнаруживать HBeAg , в дальнейшем сероконверсия также отсутствует, что характерно для формирования ХВГВ.
Основными маркерами репликации вируса является определение в крови ДНК-HBV и фермента ДНК-полимеразы (DNA-p). Отсутствие маркеров репликации и выявление HBsAg , а нти- HBclgM и анти-НВе характерно для интегративной фазы.
Выделяют 3 серологических варианта хронического вирусного гепатита В:
- ХВГВ с минимальной активностью;
- НВе-негативный ХВГВ;
- НВе-позитивный ХВГВ.
Хронический вирусный гепатит B с минимальной активностью. Ранее использовали термин «носительство HBsAg». Для этого серологического варианта характерно:
Наличие в сыворотке крови HBsAg
более 6 мес;
- отсутствие HBeAg
и наличие анти-НВе;
- наличие ДНК-HBV в сыворотке крови в концентрации <10 5 копий/мл (2,0-10 3 МЕ/мл);
- нормальный уровень активности АЛТ и АСТ;
- отсутствие патологических признаков воспалительных изменений по данным биопсии печени.
НВе-негативный хронический вирусный гепатит B . Для этого варианта характерны следующие маркеры:
Наличие HBsAg
;
- отсутствие HBeAg
при наличии анти-НВе
;
- концентрации вирусной ДНК-HBV >10 5 копий/мл (2,0-10 3 МЕ/мл);
НВе-позитивный вариант хронического вирусного гепатита B . В данном случае характерны такие маркеры:
Наличие HBsAg
;
- выявление HBeAg
в дальнейшем возможна спонтанная сероконверсия HBeAg
на анти-НВе;
- концентрация ДНК-HBV >10 6 копий/мл (2,0-10 4 МЕ/мл);
- обнаружение ДНК-HBV методом молекулярной гибридизации;
- повышение АЛТ в 1,5 раза от нормы;
- наличие гистологических признаков воспалительного процесса в печени.
Молекулярно-биологические методы исследования. Если серологические методы используют на первой ступени специфической диагностики вирусных поражений печени, то на второй применяют ПЦР или транскрипционную амплификацию (ТАМ). Выделяют качественные и количественные молекулярно-биологические методы. Обследование начинают с качественных методов (более чувствительны, чем количественные), целью которых является обнаружение генетического материала HBV без оценки концентрации вируса, окончательная специфическая диагностика HBV-инфекции. В основе качественных методов выявления ДНК-HBV — амплификация нуклеиновых кислот методами ПЦР или ТАМ. Если результаты качественного определения ДНК-HBV отрицательны, а анти- HBs и/или анти-НВе определяются, то возможны 3 варианта:
- концентрация ДНК вируса в крови постоянно низкая, диагностические возможности метода не позволяют ее выявить;
- получен ложноположительный результат серологического теста на антитела;
- острый период HBV-инфекции закончился, хронизации не произошло, антитела отражают наличие иммунитета после перенесенной инфекции.
При получении положительного результата качественного молекулярно-биологического метода переходят к проведению количественного для определения концентрации ДНК-HBV в крови. Если качественный молекулярно-биологический метод уточняет диагноз вирусной HBV-инфекции, то количественный важен для определения тактики ведения больных. В количественном определении генома вируса используют ПЦР или ТАМ, а также амплификацию сигнала (метод разветвленной ДНК). Для оценки количества вируса в крови принято использовать стандартизированные единицы — ME/мл. Количественные методы определения ДНК-HBV позволяют определить целесообразность проведения противовирусной терапии. При уровне ДНК-HBV меньше 2,0-10 3 ME/мл (10 5 копий/мл) ПВТ не проводится.
В настоящее время распространена ПЦР в реальном времени (Real-Time PCR), которая решает проблему контаминации на заключительном этапе «стандартной» ПЦР как причины ложноположительных результатов. Используют флуоресцентномеченые олигонуклеотидные зонды (ФМ-зонды), которые добавляют в ПЦР-смесь. При появлении специфического продукта амплификации они образуют с ним комплекс, вызывая повышение уровня флуоресцентного сигнала. Real-Time PCR дает возможность:
Количественной оценки ЦИК-HBV в крови;
- контроля уровня вирусной репликации у больных с ХВГВ с минимальной активностью и концентрацией ДНК-HBV менее2,0-10 3 ME/мл (10 5 копий/мл);
- оценки эффективности ПВТ.
Сегодня у больных, получающих многочисленные трансфузии компонентов крови, используется мультиплексная диагностика HBV, HCV, парвовируса В19 (ПВ В19). Последний в состоянии иммуносупрессии часто приводит к анемии и парциальной красноклеточной аплазии костного мозга. Система для мультиплексной Real-Time PCR основана на прохождении реакций в формате Такман (Taqman) с наличием двух праймеров и флуоресцирующего зонда. Для каждого из трех вирусов в целях внутреннего контроля подобраны соответствующие пары праймеров и зонды. Затраты времени от момента взятия образцов компонентов донорской крови до получения окончательных результатов составляют не более 4 ч. Тестирование донорской крови на серологические маркеры HBV, HCV, ПВ В19 не исключает возможности их инфицирования. В связи с этим мультикомплексная диагностика для мониторинга указанных инфекций важна у данной категории больных.
Генотипирование. Генетическая вариабельность HBV влияет на клиническую картину, течение и прогноз ХВГВ. Восемь основных типов HBV обозначают буквами латинского алфавита от А до Н. Определены регионы распространения каждого генотипа вируса. Тяжелее протекает ХВГВ с генотипами C и D . Генотип D HBV характеризуется наименьшей чувствительностью к ПВТ. Проведение генотипирования дает возможность прогнозировать в определенной мере эффективность лечения, клиническое течение и исходы.
Определение стадии фиброза
Пункционная биопсия печени (ПБП) позволяет на основании морфологического исследования определить стадию фиброза, при нескольких ПБП в динамике проводить мониторинг эффективности ПВТ при ХВГВ. В основном ПБП используют у больных перед началом курса этиотропного лечения. ПБП с морфологическим исследованием помогает не только уточнить диагноз, но и определить активность и стадию процесса, контролировать эффективность лечения. ПБП в динамике (через 3-5 лет) проводят для оценки темпов прогрессирования ХВГВ, развития фиброза и цирроза печени. Оптимальный для исследования биоптат печени должен иметь длину столбика не менее 15-20 мм с наличием не менее 5 портальных трактов.
Основные показания к проведению ПБП: хронический гепатит и цирроз печени; внутрипеченочный холестаз (дуктопения); болезни накопления; лекарственный гепатит; портальная гипертензия и врожденный фиброз печени; очаговые поражения печени (биопсия под контролем методов визуализации); трансплантация печени (для диагностики реакции отторжения); гепатомегалия или спленомегалия неясного генеза; повышение уровня аминотрансфераз неуточненной этиологии; жировой гепатоз.
Необходимые исследования перед биопсией:
Общий анализ крови с обязательным подсчетом количества тромбоцитов;
- протромбиновый индекс, протромбиновое время, активированное частичное тромбопластиновое время, фибриноген;
- УЗИ органов брюшной полости;
- определение группы крови и резус-фактора;
- агрегационная способность тромбоцитов;
- компьютерная томография печени (при выявлении очаговых изменений в печени).
Ультразвуковая допплеросонография позволяет измерить диаметр и площадь поперечного сечения воротной и селезеночной вен с одновременным определением скоростных показателей (максимальная линейная и объемная скорости) кровотока в них. Указанные показатели изменяются преимущественно при стабильно высоком портальном давлении (ПД), в основном у больных с циррозом печени. У пациентов с минимальной активностью ХВГВ в динамике не наблюдается существенного расширения диаметра портальной и селезеночной вен, а величина ПД близка к норме. У больных с высокой активностью воспалительного процесса диаметр воротной и селезеночной вен и уровень ПД увеличиваются. При повышении ПД снижается скорость кровотока в воротной вене. В клинической практике о степени портальной гипертензии (ПГ) судят по диаметру воротной и селезеночной вен. В большинстве случаев существует прямая коррекция между уровнем ПД и диаметром воротной вены. Однако такая взаимосвязь наблюдается не всегда. В изменении параметров печеночной гемодинамики при ХВГВ активность воспалительного процесса играет ведущую роль. Динамика клинических симптомов, лабораторных показателей, УЗИ печени, параметры гепатопортального кровотока по данным УЗИ позволяют в определенной мере судить о результатах проведенного комплексного лечения. Стабильные показатели диаметров портальной и селезеночной вен, отсутствие повышения в динамике ПД дают возможность считать проведенное лечение эффективным.
УЗИ-режим позволяет определить:
Плотность ткани (MG —
Mean
Gray
Value
)
по серой шкале;
- индекс кровотока (FVI
—
Flow
Vascularization
Index
)
— объем крови, проходящий через исследуемый объем печени (мл/мин);
- индекс васкуляризации (VI
—
Vascularization
Index
)
, отражающий содержание сосудистых элементов в объеме печеночной ткани;
- индекс текучести (FI
—
Flow
Index
)
— интенсивность кровотока.
Эластография — это метод исследования эластичности печени с использованием аппарата FibroScan, позволяющий определять степень фиброза печени и наличие цирроза у больных с хроническими заболеваниями печени. Используется ультразвуковой датчик с источником колебаний средней амплитуды и низкой частоты (50 Гц). Скорость распространения упругих волн в ткани печени прямо пропорциональна степени фиброза. Метод не имеет противопоказаний, однако не используется при ожирении и наличии асцита. Эластография является неинвазивным альтернативным методом оценки фиброза печени, что особо значимо при наличии противопоказаний к проведению ПБП или отказе больных от ее проведения. Сегодня остаются не до конца разрешенными два вопроса: 1) как можно использовать результаты эластографии в целях контроля над прогрессированием заболевания? и 2) достаточно ли чувствительна эластография для определения выраженности фиброза печени в течение длительного времени, особенно на фоне противовирусной и антифибротической терапии? Продолжается внедрение МР-эластографии. Данный метод как и его УЗ-аналог, позволяет картировать печень в зависимости от разницы в плотности тканей.
Определение сывороточных маркеров фиброза печени (показателей внеклеточного соединительнотканного матрикса) можно использовать в клинической практике для контроля эффективности ПВТ, динамического наблюдения за прогрессированием фиброза печени, если нет возможности повторного проведения ПБП. Необходима комплексная оценка биохимических показателей внеклеточного матрикса у больных с ХВГВ с учетом всех звеньев, участвующих в метаболизме коллагена — коллагеназы, ингибитора протеиназ — α 1 -протеиназного ингибитора (α 1 -ПИ), продуктов метаболизма коллагена — фракции оксипролина. Ни по одному из этих показателей в отдельности невозможно адекватно оценить степень фиброза, тем не менее одновременное определение может быть достаточно информативным. Диагностическое и прогностическое значение имеют определение сывороточного гликопротеина YKL-40 у больных с умеренным и тяжелым фиброзом печени. Неинвазивные методы диагностики фиброза печени пока еще не получили широкого применения в клинической практике. К ним относится и проведение дыхательных тестов с соединениями, меченными углеродом 13 С, такими как галактоза и аминопирин.
При лечении больных с ХВГВ для врача является важным определение выраженности фиброза печени в целях прогноза течения болезни и оценки проводимого лечения. Приведенные методы определения стадии фиброза печени (см. табл. 1, п. 1-5) не всегда доступны, довольно трудоемкие и дорогостоящие. В определенной мере для альтернативной оценки степени фиброза в стадии цирроза печени могут использоваться диагностические шкалы. С их помощью при комплексной оценке некоторых параметров можно косвенно оценить степень фиброза печени. Для определения фиброза в стадии цирроза печени используют дискриминантную счетную шкалу (ДСШ), предложенную М. Bonacini в 1997 г.. Данная шкала предполагает использование 3 параметров: количество тромбоцитов, величину международного нормализованного отношения (МНО) и соотношение АЛТ/АСТ (табл. 2). Ее специфичность в определении стадии фиброза составляет 98%, чувствительность — 46%. Динамика МНО определяется снижением синтетической функции печени вследствие прогрессирования фиброза. Уменьшение соотношения АЛТ/АСТ свидетельствует о более тяжелом повреждении гепатоцитов с освобождением основной (митохондриальной) фракции ACT, что приводит к снижению соотношения АЛТ/АСТ до 0,6. Эти изменения характерны для выраженного диффузного воспалительного процесса в печени с прогрессированием фиброза. Уменьшение количества тромбоцитов в процессе фиброгенеза печени определяется снижением синтеза тромбопоэтина, активацией тромбоцитов и гиперспленизмом на стадии цирроза печени. У больных с суммой баллов по ДСШ 7 и более с высокой вероятностью предполагается фиброз III—IV стадии. Соответствие индекса фиброза (ИФ) по ДСШ стадиям фиброза по METAVIR и ISHAK представлено в табл. 3.
|
Параметр |
Количество баллов |
||||||
|
АЛТ/АСТ, ед |
|||||||
|
Тромбоциты, 109/л |
|||||||
|
Интенсивность фиброза |
Стадия фиброза |
||
|
Умеренный |
|||
Оценка ИФ по ДСШ у пациентов с хроническим гепатитом различной этиологии дает возможность с высокой точностью оценить стадию фиброза печени. Учитывая низкую стоимость исследования, доступность методики определения ИФ по ДСШ, она может быть широко использована как врачами поликлиник, так и стационаров. Особенно важно оценить динамику фиброзообразования в печени при отсутствии возможности проведения ПБП.
Обследование для решения вопроса о возможности проведения противовирусной терапии
Проведение этого заключительного этапа обследования целесообразно, если больному будет проводиться ПВТ.
Обследование структурного и функционального состояния щитовидной железы назначается для исключения прежде всего аутоиммунного тиреоидита. Тяжелое течение этого заболевания чаще является противопоказанием к проведению ПВТ. Любое заболевание щитовидной железы, если оно протекало в тяжелой форме, на фоне ПВТ может прогрессировать. В то же время эффективность ПВТ снижается. Если при УЗИ не определяются изменения в щитовидной железе, ограничиваются исследованием уровня ТТГ. При нормальных значениях этого гормона дальнейшее исследование функции железы можно не проводить. В случае выявления неоднородности паренхимы при УЗИ и/или изменении уровня ТТГ необходимо дополнительное обследование. При этом определяют следующие показатели: общий тироксин (Т 4), свободный тироксин (сТ 4), общий трийодтиронин (Т 3), антитела к тиреоидпероксидазе, антитела к тиреоглобулину. При нарушении функции щитовидной железы больной должен быть осмотрен эндокринологом, решение о возможности проведения ПВТ принимается совместно с этим специалистом.
Определение ANA — скрининговый тест выявления наличия гетерогенных антител к различным структурам ядер клеток. При высоких титрах ANA необходимо исключать диффузные заболевания соединительной ткани. У 10% здоровых людей ANA обнаруживается в титре <1:50. При ХВГВ могут определяться ANA в титрах не более 1:200-1:400, при этом эффективность ПВТ снижается.
Определение уровня сывороточного железа. Повышение уровня сывороточного железа может наблюдаться при гемохроматозе, циррозе, выраженном фиброзе печени. Если показатель сывороточного железа превышает нормативные значения, определяется коэффициент насыщения трансферрина железом. При значениях >55% необходимо исключить гемохроматоз. Повышение содержания сывороточного железа при значениях коэффициента насыщения трансферрина от 20 до 55% (норма) чаще обусловлено тяжелым диффузным поражением печени с формированием выраженного фиброза или цирроза. При этом эффективность ПВТ будет ниже.
Альфа-фетопротеин (АФП) — онкомаркер для выявления и мониторинга гепатоцеллюлярной карциномы. Его уровень необходимо определять у больных с выраженным фиброзом и циррозом печени.
Обследование для исключ ения других более редких гепато тропных вирусов (TTV , HGV , SEN ). При проведении скринингового исследования определяют наличие антител к этим вирусам ИФА, при положительном результате проводят ПЦР для подтверждения наличия ДНК-вируса.
Определение уровня криоглобулинов в крови. Смешанная криоглобулинемия вторичного характера может наблюдаться при хронических вирусных гепатитах. В сосудистом русле образуются криоглобулины, которые представляют собой циркулирующие иммунные комплексы (ЦИК), состоящие из IgM — ревматоидного фактора и поликлонального Ig G . Криоглобулины способны к аномальному осаждению при температуре ниже 37°С (криопреципитация). При исследовании крови определяется выраженная вариабельность уровня СОЭ и уровня гамма-глобулинов. При отсутствии возможности выявления криоглобулинов в сыворотке крови выявляют ревматоидный фактор. Их определение в средних или высоких титрах у пациента с ХВГВ существенно повышает вероятность криоглобулинемии (неполного криоглобулинемического синдрома). Криоглобулинемический васкулит (полный криоглобулинемический синдром) предполагает наличие клинических симптомов васкулита и криоглобулинемии. Существование криоглобулинемического синдрома у больного снижает эффективность ПВТ.
Исследование на герпесвирусы. Данное исследование включает определение в сыворотке крови ДНК герпесвирусов, которые могут вызывать прогрессирование диффузного воспалительного процесса в печени.
Иммунограмма. У больных с ХВГВ может определяться иммунная недостаточность. Оценивается склонность к аутоиммунным реакциям, о которой могут свидетельствовать повышение уровня ЦИК и аутоантител (ревматоидный фактор, ANA и др.), выявление криоглобулинов.
Основными причинами фиброза печени являются гепатиты B и C , злоупотребление алкоголем, среди других факторов — иммуноопосредованные повреждения, генетические аномалии, неалкогольный стеатогепатит, который чаще развивается на фоне сахарного диабета и метаболического синдрома. Раннее выявление ХВГВ дает возможность своевременно назначить эффективное лечение, которое снизит темпы прогрессирования фиброза печени и вероятность формирования цирроза. Более широкое применение экспресс-диагностики HBV-инфекции позволяет своевременно выявить заболевание. Однако использование эластографии, сывороточных маркеров фиброза, ИФ с определением баллов по ДСШ, гистологического исследования после ПБП дают возможность проводить длительный мониторинг стадий фиброза печени. Соблюдение этапности в обследовании больных с ХВГВ позволяет своевременно выявлять HBV-инфекцию, осуществлять длительное динамическое наблюдение за клиническим течением заболевания, улучшать прогноз и качество жизни больных.
И.В. Евстигнеев
Возбудитель гепатита В - ДНК-содержащий вирус, выявляется в ткани печени и сыворотке крови в виде сферических структур диаметром 42 мм - частица Дейна. Вирус обладает тремя антигенными детерминантами. С внешней оболочкой вируса связан поверхностный антиген вируса гепатита В (HBsAg), с сердцевинной частью частицы Дейна - сердцевинный антиген (HBcAg) и HBeAg, являющийся его субъединицей. ДНК генома HBV представлена двойной циркулярной спиралью, одна из которых неполная и может быть завершена соответствующими нуклеотидами, доставленными посредством ДНК-зависимой ДНК-полимеразы. Геном HBV может существовать в эписомальной (свободной) и хромосомальной (интегрированной) формах. Были выделены две биологические фазы развития HBV: ранняя репликативная и поздняя интегративная. В раннюю фазу HBV-инфекции занесенные в кровь частицы Дейна проникают через мембрану гепатоцита, ДНК HBV транспортируется к ядру гепатоцита, где с участием вирусной ДНК-полимеразы идет интенсивная наработка ДНК HBV, а также кодируются и синтезируются все вирусные субкомпоненты (HBcAg, HBeAg, HBsAg) с последующей сборкой полного вириона.
В сыворотке крови в репликативную фазу циркулируют наряду с HBsAg, HBeAg, анти-HBc IgM и ДНК HBV-полимераза, которые признаны сывороточными маркерами фазы репликации HBV. В тканях печени выявляются ДНК HBV и HBcAg. Во время этой фазы возможна элиминация HBV как спонтанная, так и при использовании химиотерапевтических противовирусных средств и интерферона.
Репликацией HBV в гепатоцитах связаны активность (некрозы гепатоцитов) и прогрессирование патологического процесса в печени. Продолжительность этой фазы при хронических гепатитах составляет от 6 месяцев до 10 и более лет. У 10% больных ежегодно отмечается спонтанное прекращение репликации HBV. Последнее наблюдается также при формировании ЦП и суперинфекции вирусами гепатита Д и С.
На более поздних стадиях развития HBV-инфекции происходит интеграция фрагмента ДНК вируса, несущего гены HBsAg в ДНК гепатоцита с последующим кодированием и синтезом преимущественно HBsAg с участием ДНК-полимеразы гепатоцита. Рядом исследователей показано, что вирусная ДНК может быть интегрирована не только в клетки печени, но и в клетки поджелудочной и слюнных желез, кожи, почек. ДНК HBV была выявлена в лейкоцитах периферической крови, в сперматозоидах, мононуклеарных клетках, в слюне, моче больных хроническими заболеваниями печени как с наличием маркеров репликации HBV, так и с их отсутствием. В эту, так называемую интегративную, фазу полная репликация вируса прекращается. У таких больных становится невозможной ликвидация HBsAg-носительства.
О переходе репликативной фазы в интегративную свидетельствует сероконверсия HBeAg в HBeAb, исчезновение из сыворотки крови ДНК HBV, ДНК-полимеразы и HBcAg из ткани печени. Интеграция генома HBV в геном гепатоцита сопровождается наступлением клинической и гистологической ремиссии хронических заболеваний печени вплоть до формирования хронического бессимптомного носительства HBsAg с минимальными измененями ткани печени. Состав сывороточных и тканевых маркеров HBV представлены в таблице 7.
Таблица 7. Маркеры вируса гепатита В в репликативную и интегративную фазу развития НВV-инфекции
Маркеры HBV Фаза развития HBV-инфекции
репликации интеграции
I. Сывороточные HBsAg HBeAg ДНК HBV HBcAb IgM HBcAb IgG HBsAb HBeAb II. Тканевые HBcAg HBsAg ДНК HBV + + + + - - - + + + + - - - + - + - + -
Клинические варианты хронической HBV-инфекции включают: хронический активный гепатит (ХАГ В), хронический персистирующий гепатит (ХПГ В), хронический лобулярный гепатит (ХЛГ В), асимптоматическое ("здоровое") носительство HBsAg, цирроз печени (ЦП), первичный рак печени (ПРП), узелковый периартериит (Рисунок 2).
Рисунок 2. Клинические варианты HBsAg-носительства
HBsAg - носитель
ХАГ ХПГ ХЛГ АСИМПТОМАТИЧЕСКОЕ НОСИТЕЛЬСТВО
ВЫЗДОРОВЛЕНИЕ ?
ЦИРРОЗ ПЕЧЕНИ ПЕРВИЧНЫЙ РАК ПЕЧЕНИ
СМЕРТЬ
Состав сывороточных маркеров HBV при различных клинико-морфологических формах хронической HBV-инфекции представлены в таблице 8.
Таблица 8. Соотношение профилей сывороточных маркеров HBV с активностью патологического процесса в печени
Профили сывороточных маркеров HBV Фаза развития HBV-инфекции Активность Предположительный диагноз
1 HBsAg+, HBeAg+, ДНК HBV+ репликация имеется ХАГ, ХЛГ, ЦП
2 HBsAg+, HBeAg-, анти-HBe-, ДНК HBV+ репликация имеется ХАГ, ЦП
3 HBsAg+, анти-HBe+, ДНК HBV+ репликация, или интеграция, или их сосуществование имеется ХАГ, ЦП, ПРП
4 HBsAg+, анти-HBe+, ДНК HBV- интеграция отсутствует асимптоматическое носительство HBsAg, ЦП, ПРП
5 HBsAg-, анти-HBe+, ДНК HBV+ преобладание интеграции незначительная или отсутствует ХПГ, (ХАГ), ЦП
6 HBsAg-, анти-HBe+, ДНК HBV- ? отсутствует нормальная печень, неактивный ЦП
7 анти-HBs+, анти-HBe+, анти-НВс+ ? отсутствует или незначительная нормальная печень, ЦП, ХПГ
Примечание: ЦП - цирроз печени
ГЦП - гепатоцеллюлярная карцинома
Catad_tema Вирусные гепатиты - статьи
Клиническое значение и трудности диагностики латентной HBV инфекции
Опубликовано в:Информационный бюллетень
Д. Т. Абдурахманов, Кафедра терапии и профессиональных болезней ММА им. И. М. Сеченова
Как известно, при хронической вирусной инфекции для персистирования вирусы используют различные механизмы, среди которых наиболее важными являются нецитопа тический способ репликации в клетках организма хозяина и возможность формирования латентного состояния, позволяющего вирусу избегать иммунного надзора . В последние годы благодаря достижениям молекулярной биологии латентная вирусная инфекция привлекает все большее внимание. Классическим примером латентной инфекции является вирус простого герпеса, который, как установлено, может длительное время сохраняться в клетках нервной системы, не экспрессируя свои антигены, что делает его недоступным для иммунной системы . В настоящее время возможность формирования латентной инфекции установлена и для вируса гепатита В (HBV). Клинико-биологическое значение и механизмы формирования латентной HBV инфекции, а также трудности ее диагностики изучаются в настоящее время достаточно интенсивно и являются предметом дискуссий. В данном обзоре мы попытались представить современное состояние этой проблемы.
До настоящего времени хроническая HBV инфекция определялась как наличие в сыворотке крови поверхностного антигена HBV (HBsAg) в течение более 6 мес. после инфицирования, при этом термин "хроническая инфекция" включает в себя различные варианты сосуществования микро- и макроорганизмов. При HBV инфекции спектр и выраженность клинических проявлений зависят от взаимоотношений вируса и иммунной системы хозяина, варьируя от бессимптомного носительства вируса до тяжелого поражения различных органов и систем, прежде всего печени, но при всех формах хронической HBV инфекции обязательным ее условием являлось наличие в сыворотке крови HBsAg. Исчезновение HBsAg и появление антител к нему рассматривалось как признак освобождения организма от вируса, т.е. прекращения инфекции.
Однако в последние годы установлено, что у ряда больных, несмотря на отсутствие HBs-антигенемии и наличие anti-HBs, в ткани печени и сыворотке крови может обнаруживаться ДНК вируса (HBVDNA) . При этом в сыворотке либо выявляли маркеры перенесенной HBV инфекции (антитела к антигенам вируса, прежде всего "изолированные" anti-HBc), которые, как теперь считают, могут быть признаком хронической латентной HBV инфекции, либо имело место отсутствие всех маркеров HBV (серонегативная инфекция) . Клинико-морфологические исследования более ранних лет свидетельствовали об идентичности активности и стадии печеночного процесса у больных хроническими заболеваниями печени с наличием "изолированных" anti-HBc и у больных с HBs-антигенемией . Отсутствие сывороточных маркеров персистирования вирусной инфекции (HBsAg и/или HBeAg) при сохранении вируса в организме объясняют двумя основными причинами: очень низкой репликативной активностью вируса, вследствие чего экспрессия вирусных антигенов значительно подавлена ; и наличием мутаций в геноме вируса, ведущих к нарушению синтеза вирусных антигенов, а также изменению их структуры, прежде всего HBsAg (HBsAg-мутантный штамм), что препятствует выявлению антигенов в крови доступными тест-системами . Механизмы развития низкоуровневой репликации HBV остаются неизученными, хотя известно, что суперинфекция вирусом гепатита D и/или С может оказывать ингибирующее влияние на репликацию HBV, что приводит к снижению уровня виремии HBV и клиренсу HBeAg, а в случае с HCV клиренсу не только HBeAg, но и HBsAg . Также отмечено, что алкоголь может вмешиваться в механизмы репликации вируса, и у лиц, злоупотребляющих алкоголем, часто единственным маркером хронической HBV инфекции являются anti-HBc . Аналогичное влияние на HBV характерно, в ряде случаев, и для вируса иммунодефицита человека (HIV). Так, в одном из исследований у 43% HIV-инфицированных в крови выявлялись anti-HBc, как единственный маркер сопутствующей HBV инфекции, при этом у 90% из них в сыворотке определялась HBVDNA .
В отсутствие других факторов большое значение в формировании низкоуровневой репликации HBV отводят мутациям в различных участках генома вируса, прежде всего в области перекреста С и Х генов, ответственных за репликацию вируса .
В связи с этим возникает вопрос о роли латентной HBV инфекции в развитии хронических диффузных поражений печени. Ряд авторов отмечают, что наличие латентной HBV инфекции у больных хроническим гепатитом С связано с более тяжелым течением болезни и низким ответом на противовирусную терапию . Улиц с алкогольным поражением печени наличие "изолированных" anti-HBc обусловливает неблагоприятный прогноз вследствие повышенного риска развития цирроза печени и гепатоцеллюлярной карциномы .
Несомненным фактом является то, что больные латентной HBV инфекцией могут быть источниками вируса и отвечать за развитие посттрансфузионного гепатита и инфицирование реципиентов донорских органов, особенно печени. Так, отмечены случаи, когда переливание крови и трансплантация органов от anti-HBc/anti-HBs позитивных доноров приводит к инфицированию реципиентов . Это связано с тем, что скрининг на HBV основывается на выявлении HBsAg, который не обнаруживается в случаях латентной инфекции, а также с тем, что обычные методы ПЦР не способны выявлять низкий уровень виремии. Широко обсуждается роль латентной HBV инфекции в развитии цирроза печени и гепатоцеллюлярной карциномы. Установлено, что, несмотря на клиренс HBsAg, возможно прогрессирование болезни вплоть до гепатоцеллюлярной карциномы . Если развитие гепатоцеллюлярной карциномы объясняют интеграцией генома вируса в геном клеток печени с последующей активацией про-онкогенов и подавлением опухоль-супрессорных генов, главным образом р53 (один из возможных механизмов развития рака печени), то патогенез повреждений печени при латентной вирусной инфекции остается неясным. В ряде исследований у больных с поражением печени неизвестной этиологии, имеющих признаки умеренной и высокой активности воспалительного процесса и далеко зашедшего фиброза в отсутствие серологических маркеров HBV инфекции, при использовании высокочувствительных методов ПЦР - "nested" PCR - в сыворотке выявлялась HBVDNA, а при иммунногистохимическом исследовании в ткани печени - антигены HBV . Это позволяет обсуждать роль латентной HBV инфекции в развитии криптогенных поражений печени, хотя сами авторы не исключают этиологическое значение еще неизвестных гепатотропных вирусов.
Известно, что длительная иммунносупрессивная терапия (химиотерапия опухолей, лечение аутоиммунных заболеваний, профилактика реакции отторжения трансплантата), прежде всего применение глюкокортикостероидов, может привести к реактивации латентной HBV инфекции, вплоть до развития фульминантного гепатита с летальным исходом . В патогенезе реактивации латентной HBV инфекции на фоне иммунносупрессивной терапии основное значение придают действию глюкокортикостероидов. Так, известно, что геном HBV содержит глюкокортикоид-чувствительные участки, активация которых усиливает репликацию вируса, продукцию и экспрессию вирусных антигенов на поверхности гепатоцитов . При этом поражение печени в ходе терапии глюкокортикостероидами обусловлено прямым цитопатическим действием вируса - усиленный синтез вирусных антигенов, прежде всего HBsAg, приводит к их избыточному накоплению в цитоплазме клеток печени, с последующей дистрофией, некрозом гепатоцитов и развитием тяжелого холестатического поражения печени. В качестве примера можно привести особую клиническую форму хронического гепатита В - фиброзирующий холестатический гепатит, развивающийся у лиц, которым после трансплантации печени длительно проводят иммунносупрессивную терапию глюкокортикостероидами . Эта форма хронического" гепатита В по своим клинико-морфологическим признакам похожа на поражение печени при дефиците а l-антитрипсина, что, по-видимому, связано с общностью генеза поражения гепатоцитов: в первом случае в клетке накапливается HBsAg, во втором а l-антитрипсин. Поражение печени возможно и при резкой отмене глюкокортикостероидов, когда на фоне прекращения иммунносупрессивного действия глюкокортикостероидов и в ответ на повышенную экспрессию вирусных антигенов на поверхности гепатоцитов, прежде всего HBcAg, происходит иммунноопосредованный цитолиз гепатоцитов цитотоксическими лимфоцитами - так называемый синдром "рикошета".
"HBsAg-мутантная" инфекция (при которой в крови циркулирует структурно-измененный поверхностный антиген) представляет серьезную опасность для населения. Во-первых, она является потенциальным источником заражения реципиентов крови и донорских органов, так как во многих странах мира HBsAg является основным и единственным скрининговым маркером HBV-инфекции. Во-вторых, "HBsAg-мутантный" штамм является серьезной проблемой для программ вакцинации, так как вакцин-индуцированные антитела не обеспечивают иммунитет от инфицирования HBsAg-мутантным штаммом ("вакцин-ускользающий штамм"). У таких пациентов, несмотря на наличие в сыворотке anti-HBs, инфицирование такими штаммами может вызвать гепатит В. Данный штамм может также привести к реинфицированию печени в посттрансплантационном периоде, несмотря на профилактику специфичным иммуноглобулином (HBIg), который представляет собой поликлональные антитела к основным эпитопам поверхностного антигена HBV. Вследствие изменения структуры поверхностного антигена у HBsAg-мутантного штамма, антитела неспособны нейтрализовать вирус и предотвратить развитие инфекции.
Таким образом, анализ результатов исследований, посвященных этой проблеме, позволяет охарактеризовать латентную HBV инфекцию как гепатит В с наличием показателей репликации вируса (обнаружение HBV DNA в сыворотке крови и/или ткани печени) при отсутствии других серологических маркеров, указывающих на персистирование вируса (прежде всего негативный результат выявления HBsAg). Можно выделить два варианта латентной HBV инфекции. При первом, низкий уровень репликации HBV и, как следствие, пониженный синтез и экспрессия вирусных антигенов обусловлены влиянием ряда факторов: адекватного ответа иммунной системы; ингибирующего влияния на HBV других вирусов /HCV, HDV, HIV/; мутаций в определенных участках генома вируса, ответственных за его репликативную активность. При втором варианте репликация вируса не подавлена, HBsAg синтезируется и экспрессируется, но не выявляется современными коммерческими тест-системами вследствие мутаций, изменяющих структуру его основных детерминант.
До настоящего времени остаются неясными патогенетические механизмы развития поражений печени при латентной HBV инфекции. Каким образом столь низкая репликативная активность вируса может вызывать воспалительные изменения в печени? Служит ли выявление латентной HBV инфекции у больных с криптогенными заболеваниями печени доказательством ее этиологической роли или она лишь фон, пусть и неблагоприятный, на котором реализует свое действие какой-либо еще неизвестный агент? Кроме того, требует своего изучения и возможная триггерная роль латентной HBV инфекции в развитии аутоиммунного гепатита, при котором могут выявляться антитела к HBV, в том числе "изолированные" anti-HBc.
Учитывая возросшее значение и роль латентной HBV инфекции в развитии поражений печени, весьма актуальной становится разработка доступных, воспроизводимых и чувствительных способов ее диагностики. Появление в широкой клинической практике диагностических препаратов, способных выявлять мутантные формы вируса гепатита В и его антигены, способствовало бы более углубленному изучению патогенетических механизмов формирования латентной HBV инфекции и ее роли в развитии болезней печени.
Литература:
1. Апросина З.Г., Лопаткина Т.Н., Яковенко Э.П. и др. Характеристика хронических заболеваний печени с наличием сывороточных маркеров вируса гепатита В. // Тер. архив.-1988.-№ 11 .-С.23-28.
2. Сюткин В.Е. Клиническая характеристика хронических заболеваний печени, обусловленных сочетанной инфекцией вирусами гепатита В, С и/или дельта. // Автореферат дисс. канд. мед. наук, Москва, 1999.
3. Танащук Е.Л., Апросина З.Г, Секамова С.М., Попова И.В. Клинико-морфологическая характеристика, особенности течения хронических заболеваний печени у больных, злоупотребляющих алкоголем и инфицированных вирусами гепатита. // Рос. журн. гастроэнтерол., гепатол., колопроктол.- 2001.- Т. 11, №1, прил. №12.-С.38,№120.
4.BennerK.G., Lee R.G., Keefe E.B. etal. Fibrosing cytolitic liver failure secondary to recurrent hepatitis В after liver transplantation. // Gastroenterology.- 1992. -Vol. 103.-P.1307-12.
5. Borrow P. Mechanisms of viral clearance and persistence. //J Viral Hepatitis, 1997, 4 (Sup 2), 16-24.
6. Brechot С., Degos R, Lugassy С. et al. Hepatitis В DNA virus in patients with chronic liver disease and negative tests for hepatitis В surface antigen. // N EngiJ Med.- 1985.-Vol.312.-p.270.76.
7. Cacciola I., Pollicino Т., Squadrito G. et al. Occult hepatitis В virus infection in patients with chronic hepatitis С liver disease. // N Engi J Med.-1999.-Vol.341,NL-p.22-26.
8. Cacciola I., Pollicino Т., Squadrito G. et al. Quantification ofintrahepatic hepatitis В virus DNA in patients with chronic HBV infection. // Hepatology.-2000.-Vol.31,N2.-p.508-11.
9. Carman W.F. The clinical significance of surface antigen variants of hepatitis В virus. // J Viral Hepatitis.-1997.-Vol.4(Suppl).-p.l 1-20.
10. Chazouilleres 0., Mamish D., Kim M. et al. "Occult" hepatitis В virus as a source of infection in liver transplant recipients. // Lancet.-1994.-Vol.343.-p. 142-46.
11. Chemin 1., Zoulim F., Merle P. et al. High incidence of hepatitis В infections among chronic hepatitis cases of unknown aetiology. // J Hepatology. -2001.-Vol.34,N3.-p.447-54.
12. Chou C-K., Wang L-H., Lin H-M., Chi C-W. Glucocorticoid stimulates hepatitis В viral gene expression in cultured human hepatoma cells. // Hepatology-1992.-Vol.l6.-p.l3-18.
13. Davies S.E., Portmann B.C., Grady J.G. et al. Hepatic histological findings after transplantation for chronic hepatitis В virus infection, including a unique pattern of fibrosing cholestatic hepatitis. // Hepatology.-1991.-Vol. 13.-p. 150-07.
14. Dickson R.C., Everhart J.E., Lake J.R. et al. Transmission of hepatitis В by transplantation of livers from donors positive for antibody to hepatitis В core antigen. // Gastroenterology.-1997.-Vol.ll3.-p. 1668-74.
15. Fukuda R., Ishimura N., Niigaki M. et al. Serologically silent hepatitis В virus coinfection in patients with hepatitis С virus-associated chronic liver disease: clinical and virological significance. // J Med Virol.- 1999.- Vol.58.-p.201-07.
16. Grumayer E.R., Panzer S., Ferenci P., Gadner H. Reccurrence of hepatitis В in children witn serologic evidence of past hepatitis В infection undergoing antileukemic chemotherapy. // J Hepatology.-1989.-Vol.8.-p.232-35.
17. Hofer M., Joller-Jemelka H.I., Grob P.J. et al. Frequent chronic hepatitis В virus infection in H1V-infected patients positive for antibody to hepatitis В core antigen only. Swiss H1V cohort study. // Eur J Clin Microbiol Infect Dis.- 1998.-Vol.l7.NI.-p.6-13.
18. Hoofnagle J.H., Seeff L.D., Bales Z.B., Zimmerman H.J. Type В hepatitis after transfusion with blood containing antibody to hepatitis core antigen./,/N EngiJ Med.-1978.-Vol.298.-p.1379-83.
19. Huo T.I., Wu J.C., Lee PC. et al. Sero-clearance of hepatitis В surface antigen in chronic carriers does not necessarily imply a good prognosis. // Hepatology-1998.-Vol.28.-p.231-36.
20. Krogsgaard К., Marcellin P., Trepo C. et al. Prednisolon withdrawal therapy enhances the effect of human lymphoblastoid interferon in chronic hepatitis B.//J Hepatology. -1996.-Vol.25.-p.803-13.
21. Liaw Y-F. Role of hepatitis С virus in dual and triple hepatitis virus infection. // Hepatology.-1995.-Vol.22.N4.-p. 1101-08.
22. Lok A.F, Liang R.S., Chiu E.W. et al. Reactivation of hepatitis В virus replication in patients receiving cytotoxic therapy. // Gastroenterology.-1991. -Vol. 100. -p. 182-88.
23. Loriot M.A., Marcellin P., Bismuth E. et al. Demonstration of hepatitis В vims DNA by polymerase chain reaction in the serum and the liver after spontaneous or therapeutically induced HbeAg to anti-Hbe or HbsAg to anti-HBs seroconversion in patients with chronic hepatitis B. // Hepatology. -1992.-Vol.l5.-p.32-36.
24. Marusawa H., Uemoto S., Hijikata M. et al. Latent hepatitis В virus infection in healthy individuals with antibodies to hepatitis В core antigen. // Hepatology.-2000.-Vol.31.-p.488-495.
25. Nalpas В., Pol S., Trepo V. et al. Relationship between excessive alcohol drinking and viral infections. // Alcohol Alcoholism.-1998.-Vol.33.-p.202-06.
26. Paterlini P., Gerken G., Nakajima E. et al. Polymerase chain reaction to detect hepatitis В virus DNA and RNA sequences in primary livers cancers from patients negative for hepatitis В surface antigen. //N EngiJ Med.-1990.-Vol.323.-p.80-85.
27. Pessoa M.G., Terrault N.A., Ferell L.D. et al. Hepatitis after liver transplantation: the role of the known and unknown viruses. // Liver Transpl Surg.-1998.-Vol.6.-p.461-68.
28. Scaglioni P.P., Melegari M., Wands J.R. Characterization of hepatitis В virus core mutants that inhibit viral replication. // Virology.-1994.-Vol.205.-p.! 12-20.
29. Schories M., Peters T, Rasenack J. Isolation, characterization and biological significance of hepatitis В virus mutants from serum of a patient with immunologically negative HBV infection. // J Hepatology.-2000.-Vol.33.-p.799-811.
30. Schreiber G.B., Busch M.P, Kleinman S.H., Korelitz J.J. The risk of transfusion-transmitted viral infections. // N Engi J Med.-1996.-Vol.334.-p. 1685-89.
31. ScullyL.J., SungH., Pennie R., Gill P. Detection of hepatitis В virus DNA in serum of Canadian hepatitis В surface antigen negative, anti-HBc positive individuals, using the polymerase chain reaction. // J Med Virol.-1994.-Vol.44.-p.293-97.
32. Sheen I.S., Liaw Y.F, Chu C.M., Pao C.C. Role of hepatitis С vims infection in spontaneous hepatitis В surface clearance during chronic hepatitis В virus infection.//J Infect Dis.-1992.-Vol.l65.-p.831-34. 33. Sheu J.C., Huang G.T, Shih L.N. et al. Hepatitis С and В virus in hepatitis В surface antigen-negative hepatocellular carcinoma. // Gastroenterology.-1992.-Vol.l03.-p.1322-27.
34. Shih C.M., Lo S.J., Miyamura T. et al. Suppression of hepatitis В vims expression and replication by hepatitis С virus core protein in HuH-7 cells. //J Virol.-1993.-Vol.67.-p.5823-32.
35.SteinbergJ.L.,YeoW.,ZhongS.etal. Hepatitis В virus reactivation in patients undergoing cytotoxic chemotherapy for solid tumors: precore/core mutation may play an important role. // J Med Virol.-2000.-Vol.60.N3.-p.249-55.
36. Stevens J.G. Overview ofherpesvirus latency. // Sem Virol., 1994,5, 191-196.
37. Tur-Kaspa R., Burk R.D., Shaul Y, Shafritz D.A.Hepatitis В virus DNA contains a glucocorticoid-responsive element. // Proc Nati Acad Sci USA.-1986.-Vol.83.-p.l627-31.
38. Uemoto S., Sugiyama K., Marusawa H. et al. Transmission of hepatitis В virus from hepatitis В core antibody-positive donors in living related liver
После попадания в организм вируса гепатита B заболевание последовательно проходит через несколько стадий: инфицирование, инкубационный период, острый и наконец хронически гепатит. Надо отметить, что далеко не у всех инфицированных развивается острый гепатит или болезнь переходит в хроническую стадию.
Инкубационный период
и заболевание невозможно выявить даже с помощью анализов крови.
Острый гепатит В
Симптомы острого гепатита – недомогание, слабость, тошнота, боль в суставах, повышенная температура тела, желтуха. Они могут быть не ярко выражены или отсутствовать совсем, желтухи может не быть, поэтому острую фазу гепатита диагностируют не всегда. В этот период в анализах выявляется ДНК вируса, показатели острой фазы инфекции (антигены вируса и некоторые антитела), ферменты печени значительно повышены (см. табл. 1).
У 90-95% пациентов, заразившихся вирусом гепатита В во взрослом возрасте, симптомы заболевания исчезают самостоятельно, биохимические анализы становятся нормальными, и формируется защитный иммунитет (см. график 1). У детей это происходит гораздо реже: в возрасте до 13 лет 25-50% из них не выздоравливают самостоятельно, наступает хроническое носительство вируса гепатита В.
Хроническая HBV-инфекция
Хроническая инфекция, вызванная вирусом гепатита В, может длиться годами. Наиболее тяжелые ее последствия – это формирование цирроза и рака печени. Для удобства иначе она обозначается как HBV-инфекция (HBV – англоязычная аббревиатура, «Hepatitis B Virus», что означает «вирус гепатита В»).
В настоящее время выделяют 4 фазы хронической HBV-инфекции (см. также табл. 1, в которой отражены сочетания результатов анализов, которые характерны для этих фаз).
- Стадия иммунной толерантности
- Стадия хронического HBeAg-позитивного хронического гепатита В
- Стадия хронического HBeAg-негативного хронического гепатита В
- Стадия неактивного носительства вируса гепатита В
Стадия иммунной толерантности
Характеризуется высокой активностью размножения вируса, в анализах определяется HBeAg, АЛТ в пределах нормы (график 2), при биопсии печени воспаление и фиброз отсутствуют. Такое состояние свойственно чаще всего детям, рожденным от инфицированных матерей (до 85% из них).

Стадия хронического гепатита В (HBeAg-позитивного и HBeAg-негативного).
Ключевым фактором, отличающим стадию хронического гепатита от остальных стадий хронической HBV-инфекции, является воспаление в печени, т.е. собственно гепатит. Косвенным признаком наличия воспаления в ткани печени служит повышение АЛТ и/или АСТ, а наиболее достоверным – результаты исследования ткани печени.
Хронический HBeAg-позитивный – более ранняя, а HBeAg-негативный – более поздняя стадия хронической HBV-инфекции. По мере течения болезни вирус гепатита В постоянно мутирует (т.е. меняется его генетическая структура), а под давлением иммунной системы отбираются варианты вируса, которые не вырабатывают HBeAg. Поэтому по прошествии нескольких лет (а может быть, и десятков лет) HBeAg-позитивный хронический гепатит В переходит в HBeAg-негативный.

Таким образом, на стадии хронического гепатита у пациентов определяются признаки воспаления в печени, повышены печеночные ферменты, определяются показатели размножения вируса (график 3). В результате длительной хронической инфекции может формироваться фиброз печени.
Хроническое неактивное носительство вируса гепатита В
Это особое состояние, при котором в крови есть признаки наличия вируса, однако биохимические тесты в норме, повреждение печени минимально (график 4).

Следует помнить, что хроническая HBV-инфекция – это динамический процесс. Она отличается сравнительно быстрой сменой стадий заболевания. В связи с этим требуется постоянный контроль за лабораторными и клиническими показателями.
